��Ŀ����
13��ʵ������һ����ɫ���壬���ܺ���Na2CO3��NaHCO3��NaCl�е�һ�ֻ���֣����и���ʵ����ʵ�ó��Ľ�����ȷ���ǣ�������| A�� | ȡһ�������壬�ܽ⣬����Һ��ͨ��������CO2���۲쵽�о���������˵��ԭ������һ������Na2CO3 | |
| B�� | ȡһ�������壬�ܽ⣬����Һ�м�������CaO��ĩ����ַ�Ӧ��۲쵽�а�ɫ�������ɣ�˵��ԭ������һ������Na2CO3 | |
| C�� | ȡһ�������壬�ܽ⣬����Һ�еμ�����AgNO3��Һ���۲쵽�а�ɫ�������ɣ�˵��ԭ������һ������NaCl | |
| D�� | ��ȡ3.80g���壬���������أ�����������0.620g��������ϡ�����ܽ�������壬��ַ�Ӧ���ռ���0.880g���壬˵��ԭ�����н�����Na2CO3��NaHCO3 |
���� A��̼������Һ�Ͷ�����̼���Է�Ӧ����̼�����ƣ�̼�����Ƶ��ܽ��С��̼���ƣ�
B��̼��������Һ���ܽ�Ƚ�С�����䱥����Һ�м��������ƣ���ʹ��̼�����ƾ���������
C��̼���ơ��Ȼ��ƾ����Ժ�������֮�䷴Ӧ���ɰ�ɫ������
D��������������أ��������ᣬ˵����̼�����ƹ��壬̼���������ȷֽ�Ϊ̼���ơ�ˮ�Լ�������̼������̼Ԫ���غ���Լ���������������
��� �⣺A��̼������Һ�Ͷ�����̼���Է�Ӧ����̼�����ƣ�̼�����Ƶ��ܽ��С��̼���ƣ���������Һ��ͨ��������CO2���۲쵽�о���������˵��ԭ������һ������Na2CO3����A��ȷ��
B��̼��������Һ���ܽ�Ƚ�С�����䱥����Һ�м��������ƣ���ʹ��̼�����ƾ�����������һ������̼���ƣ���B����
C��̼���ơ��Ȼ��ƾ����Ժ�������֮�䷴Ӧ���ɰ�ɫ����������Һ�еμ�����AgNO3��Һ���۲쵽�а�ɫ�������ɣ�ԭ�����в�һ������NaCl����C����
D��������������أ��������ᣬ˵����̼�����ƹ��壬̼���������ȷֽ�Ϊ̼���ơ�ˮ�Լ�������̼������������0.620g�����ݲ����������е�̼�����Ƶ�������1.68g�����ʵ�����0.02mol�����ȷֽ�õ�̼������0.01mol������̼Ԫ���غ㣬���õ��IJ��������������ܽ⣬���Եõ�������̼0.01mol��������0.44g������һ������̼����0.01mol��������ʱ��0.02mol��84g/mol+0.01mol��106g/mol=1.786g��3.8g�����Ի������Ȼ��ƹ��壬��D����
��ѡA��
���� ���⿼���йػ�ѧ����ʽ�ļ�������ʵ��ƶϣ���Ҫ�����ò����������ʵ����ʵ�Ӧ�ý�����⣬�ѶȽϴ�

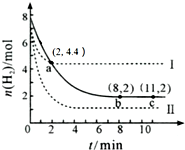
| A�� | ���¶��£�a��ʱ��3 v����CO2��=v����H2�� | |
| B�� | ���ߢ��Ӧ�������ı�����dz��뺤�� | |
| C�� | ���ߢ��Ӧ�������ı�����ǽ����¶� | |
| D�� | �ӷ�Ӧ��ʼ��a�㣬v ��CO2��=0.6 mol•L-1•min-1 |
| T���棩 | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�÷�ӦΪ���ȣ�����ȡ����ȡ�����Ӧ��
��ij�¶��£���Ӧ��ϵ�и����ʵ�ƽ��Ũ�ȷ�����ʽ��3c��CO2��•c��H2��=5c��CO��•c��H2O�������жϴ�ʱ�ķ�Ӧ�¶�Ϊ700�森
��.830��ʱ����������м���1molCO2��1molH2��ʼ��Ӧ���ﵽƽ��ʱ�����������CO2�����������25%��
���������¶Ȳ��䣬����IV��ƽ����ϵ����ͨ��2molCO2��2molH2�����ٴ���ƽ��ʱ��H2��ת����Ϊ50%��
| A�� | ���������У�PH��С | B�� | ��ˮ�����У��������α���ԭ | ||
| C�� | ��ˮ����ʱ������ת��ΪAlO2- | D�� | ���ۿ�����СӰ���ˮ���������� |
| A�� | ������ˮ��Ӧ��Cl2+H2O=2H++Cl-+ClO- | |
| B�� | ��Ũ������MnO2��Ӧ��ȡ����������MnO2+2H++2Cl-$\frac{\underline{\;��\;}}{\;}$Mn2++Cl2��+2H2O | |
| C�� | ��С�մ�����θ����ࣺHCO3-+H+=CO2��+H2O | |
| D�� | Fe3O4��ϡHNO3��Ӧ��Fe3O4+8H+=Fe2++2Fe3++4H2O |
| A�� | S | B�� | H | C�� | N | D�� | C |
