题目内容
【题目】某科研机构研发了一种以氢气为原料的新型化学电源,该电源的两个电极上分别会消耗和生成氢气,其原理如图所示,下列说法正确的是
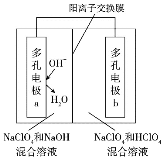
A. 电极a上发生的反应为:4OH--4e-=O2↑+2H2O
B. 电源工作时若不补充电解质两侧溶液都逐渐转化为NaClO4溶液
C. 电子从多孔电极b经导线流向多孔电极a
D. 该电源投入商用的主要难关是低成本氢气的大量获取
【答案】B
【解析】
A.两个电极分别消耗和生成氢气,根据电极a表面OH-转化为H2O可知电极a为负极,电极反应为H2-2e-+2OH-=2H2O,电极b的电极反应为2H++2e-=H2,故A错误;
B.电源工作时左侧不断消耗OH-,右侧不断消耗H+,Na+通过阳离子交换膜从左侧进入右侧,因此若不补充电解质两侧溶液都逐渐转化为NaClO4溶液,故B正确;
C.电子从多孔电极a经导线流向多孔电极b,故C错误;
D.理论上该电源两极消耗和生成的氢气的量相等,不需要消耗大量氢气,故D错误。
答案选B。

练习册系列答案
相关题目
【题目】已知断裂1mol化学键吸收的能量或形成1mol化学键释放的能量称为键能,部分物质的键能如下表所示:
化学键 | C-H | C=O | N-H | C-N | H-O |
键能(kJ/mol) | a | b | c | d | e |
甲醛制备乌洛托品的反应如下,6![]() (g) + 4NH3(g) →
(g) + 4NH3(g) →  + 6H2O(l)
+ 6H2O(l)
该反应的⊿H为 ( )
A. 6(a+b+c-d-e)kJ/molB. 6(d+e-a-b-c)kJ/mol
C. 6(b+2c-2d-2e)kJ/molD. 6(2d+2a+2e-b-3c)kJ/mol