题目内容
(8分)已知A、B、C、D是中学化学中常见的四种不同微粒。它们之间存在如图所示的转化关系。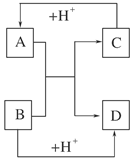
(1)如果A、B、C、D均是10电子的微粒,请写出:A的结构式________,D的电子式________。
(2)如果A和C是18电子的微粒,B和D是10电子的微粒,请写出:
①A与B在溶液中反应的离子方程式___________________________________
________________________________________________________________________。
②根据上述离子方程式,可判断C与B结合质子的能力大小是(用化学式或离子符号表示)________>________。
(3)已知肼(H2N—NH2)和甲胺(CH3—NH2)都是18个电子的分子。分析肼和甲胺的结构特点并从中受到启发,写出与其具有相同电子数的有机化合物的结构简式(至少写两个):________________________________________________________________________
________________________________________________________________________。
(1) 或H—F H········H
或H—F H········H
(2)①H2S+OH-===HS-+H2O或HS-+OH-===S2-+H2O ②OH- S2-(或HS-)
(3)CH3—CH3,CH3—OH,CH3—F(合理即可)
解析

 阅读快车系列答案
阅读快车系列答案(分)已知A、B、C、D、E五种元素都是元素周期表中前20号元素,原子序数依次增大,E的特征电子排布式为4s2。A、B、C、D四种元素在元素周期表中的相对位置如下表所示。
| …… | A | ||||||
| B | C | D |
根据以上信息,回答下列问题:
(1)元素C在元素周期表中的位置是 周期 族;D的电子排布式为: 。
(2)A和D的氢化物中,沸点较高的是 ,原因是
;A和B的离子中,半径较小的是 (填离子符号)。
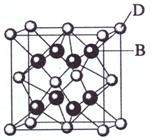
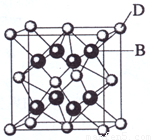
 (3) A和E可组成离子化合物,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如右图所示(阳离子用“●”表示,位于该正方体的顶点或面心;阴离子用“〇”表示,均位于小正方体中心)。该化合物的电子式是 。
(3) A和E可组成离子化合物,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如右图所示(阳离子用“●”表示,位于该正方体的顶点或面心;阴离子用“〇”表示,均位于小正方体中心)。该化合物的电子式是 。
(4)A和E化合物的晶胞1/8的体积为2.0×10-23cm3,求A和E组成的离子化合物的密度,请列式并计算(结果保留一位小数):_______________________________。
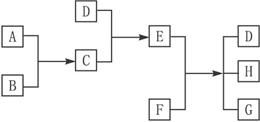
 (1)写出B的电子排布图
,C的元素符号是
,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是
;
(1)写出B的电子排布图
,C的元素符号是
,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是
;