题目内容
【题目】石油通过裂解可以得到乙烯,乙烯的产量可以用来衡量一个国家石油化工发展水平。下图是由乙烯为原料生产某些化工产品的转化关系图。

(1)乙烯生成B的反应类型是_______________________。
(2)A的名称是_______________________________ 。
(3)C中含有的官能团是 _________________________(填名称)。
(4)写出B+D→E的化学反应方程式:___________________________。
(5)写出与D同类的E的两种同分异构体的结构简式_____________;_____________。
【答案】加成 聚乙烯 醛基 CH3CH2OH + CH3COOH![]() CH3COOCH2CH3+ H2O CH3-CH2-CH2-COOH CH3-CH(CH3)-COOH
CH3COOCH2CH3+ H2O CH3-CH2-CH2-COOH CH3-CH(CH3)-COOH
【解析】
C2H4发生加聚反应得到A,A为聚乙烯,乙烯与水发生加成反应生成B,B为CH3CH2OH,乙醇在催化剂条件下发生氧化反应C,C为CH3CHO,CH3CHO可进一步氧化生成D,D为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成E,E为CH3COOCH2CH3。
(1)乙烯与水发生加成反应生成CH3CH2OH,故答案为:加成反应;
(2)C2H4发生加聚反应得到的A为聚乙烯,故答案为:聚乙烯;
(3)C为CH3CHO,含有的官能团为醛基,故答案为:醛基;
(4)反应B+D→E是乙醇与乙酸在浓硫酸、加热条件下生成乙酸乙酯,反应方程式为:CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O,故答案为:CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O,故答案为:CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(5)D(CH3COOH)属于羧酸,与D同类的E的两种同分异构体的结构简式为:CH3-CH2-CH2-COOH、CH3-CH(CH3)-COOH,故答案为:CH3-CH2-CH2-COOH;CH3-CH(CH3)-COOH。

【题目】已知马尔氏盐晶体[(NH4)2Fe(SO4)2·6H2O]易溶于水,不溶于乙醇,受热易分解,是分析化学中的重要试剂。回答下列问题:
(1)马尔氏盐晶体的制备:
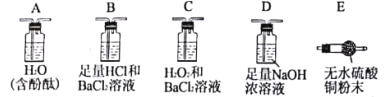
甲组同学利用新生成的硫酸亚铁溶液与硫酸铵溶液反应制备马尔氏盐晶体(已知所使用的铁屑中含有少量的Fe2O3和FeS杂质),装置如图所示;

①为了使A中所制得的FeSO4中不含Fe3+,应使______________________过量(填化学式)。
②实验前期,需要用生成的H2将装置中的空气排尽,其原因是______________________,装置B中的试剂为____________(填写试剂名称)。
③装置A中反应一段时间后,若不拆卸装置,如何使装置A中生成的FeSO4进入装置C中,叙述操作过程____________________________________________。
(2)验证马尔氏盐晶体分解的气态产物成分:
提出假设:马尔氏盐晶体分解可能生成H2O、NH3、SO3、___________等气态化合物。
实验验证:实验小组取一定量马尔氏盐晶体隔绝空气加强热分解,利用下列裝置检验气态产物的成分(防倒吸装置已略去),试完成下表:
操作步骤 | 实验现象 | 结论 |
①按___→___→____顺序连接装置(填字母)。 | ②______________________ ______________________。 | 证明气体产物中含有H2O和NH3。 |
③按B→C→D顺序连接装置,其中装置B的作用是______________________。 | B中无明显现象,C中有白色沉淀生成。 | ④_____________________ ______________________。 |
【题目】某研究性学习小组通过铁与盐酸反应的实验,研究影响反应速率的因素(铁的质量相等,铁块的形状一样,盐酸均过量),甲同学设计实验如下表:
实验编号 | 盐酸浓度(mol·L-1) | 铁的状态 | 温度/°C |
1 | 2.00 | 块状 | 20 |
2 | 2.00 | 粉末 | 20 |
3 | 1.00 | 块状 | 20 |
4 | 2.00 | 块状 | 40 |
请回答:
(1)若四组实验均以收集到500mL(已转化为标准状况下)氢气为标准,则上述实验中还需要测定的数据是________。
(2)实验________和______是研究铁的状态对该反应速率的影响(填实验编号,下同);实验______和______是研究温度对该反应速率的影响。
(3)测定在不同时间t产生氢气体积V的数据,根据数据绘制得到图,则曲线c、d分别对应的实验组别可能是_______、______。

(4)乙同学设计了下列一组实验:所用铁块的形状、质量均相同,所用酸的体积相同,其浓度如下,你认为产生氢气速率最快的是______。
A 18.4mol·L-1硫酸 B 5.0mol·L-1硝酸 C 3.0mol·L-1盐酸 D 2.0mol·L-1硫酸
【题目】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可用做供氧剂。
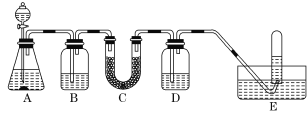
(1)A是制取CO2的装置。写出A中发生反应的化学方程式:______。
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | 除去CO2中混有的HCl |
C | Na2O2 | _______ |
D | NaOH溶液 | _______ |
(3)写出Na2O2与CO2反应的化学方程式:______。
(4)试管中收集满气体后,下一步实验操作及现象、结论是___。




