题目内容
19.A、B、C、D、E五个集气瓶中分别充满Cl2、O2、H2、HCl、HBr五种气体中的一种.其中A瓶中的气体是黄绿色.D和A气体混合见光会爆炸;B和A中的气体混合在瓶壁上出现橙红色液滴;将E瓶打开在潮湿的空气中会出现白雾.判断各为什么气体:ACl2 BHBrCO2 DH2 EHCl.分析 先根据颜色推断A;根据A、D混和见光爆炸推断D;根据B、A混和在瓶壁上出现橙红色小液滴推断B,根据E遇潮湿空气出现白雾推断E,剩下的就是C,据此答题.
解答 解:由A瓶中的气体是黄绿色,氯气是黄绿色气体,所以A是氯气;
D和A气体混合见光会爆炸,能和氯气反应的气体有H2、HBr,但氯气和HBr发生置换反应不爆炸,所以D为氢气;
B和A中的气体混合在瓶壁上出现橙红色液滴,氯气和HBr能发生置换反应生成橙红色物质溴,所以B是HBr;
E遇潮湿空气出现白雾,氯化氢遇水蒸气后能形成盐酸小液滴,所以E是氯化氢;
根据以上分析知,剩余的气体C是氧气.
故答案为:Cl2 ;HBr;O2;H2;HCl.
点评 本题以推断气体为载体考查常见气体的检验,根据气体的特殊颜色或性质判断成分,如氯气是黄绿色气体,二氧化硫能使品红褪色等,都可鉴别气体的成分,难度中等.

练习册系列答案
相关题目
9.下列说法正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 阴阳离子之间通过静电引力形成的化学键,叫离子键 | |
| C. | 在共价化合物中不可能含有离子键 | |
| D. | 含有离子键的化合物不一定是离子化合物 |
10.工业制硫酸的一步重要反应是SO2在400~500℃下的催化剂氧化:2SO2+O2?2SO3,这是一个正反应放热的反应,如果反应在密闭容器中进行.下述一个说法中错误的是( )
| A. | 实际生产中鼓入过量的空气,是为了提高SO2的转化率 | |
| B. | 即使在实际生产中鼓入过量的空气,但此过程产生的炉气中仍含有少量SO2 | |
| C. | 此反应中反应物的总能量高于生成物的总能量 | |
| D. | 使用催化剂是为了改变该化学反应的限度 |
7.香港兴建赤鱲角1248公倾新机场,是一个开山填海的庞大工程,共使用烈性炸药“TNT”5600吨.TNT炸药爆炸是时发生如下反应:21O2+4TNT=28CO2+10H2O+6N2则“TNT”的化学式是( )
| A. | C7H5N3O6 | B. | C7H5N3O4 | C. | C5H3NO6 | D. | C7H5NO6 |
14.下列化学反应的离子方程式正确的是( )
| A. | Cu溶于稀HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O | |
| B. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-═Fe(OH)2↓ | |
| C. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| D. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- |
8.分子式为C4H8O3的有机物在一定条件下具有如下性质:
①在浓硫酸存在下,能与CH3CH2OH、CH3COOH反应;
②在浓硫酸存在下,能脱水生成一种能使溴水褪色的物质,该物质只存在一种结构;
③在浓硫酸存在下,能生成一种分子式为C4H6O2的五元环状化合物;
则C4H8O3的结构简式为( )
①在浓硫酸存在下,能与CH3CH2OH、CH3COOH反应;
②在浓硫酸存在下,能脱水生成一种能使溴水褪色的物质,该物质只存在一种结构;
③在浓硫酸存在下,能生成一种分子式为C4H6O2的五元环状化合物;
则C4H8O3的结构简式为( )
| A. | HOCH2COOCH2CH3 | B. | CH3CH(OH)CH2COOH | C. | HOCH2CH2CH2COOH | D. | CH3CH2CH(OH)COOH |
9.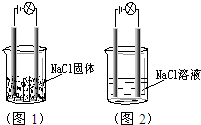 一化学兴趣小组在家中进行化学实验,按照图1连接 好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
一化学兴趣小组在家中进行化学实验,按照图1连接 好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
 一化学兴趣小组在家中进行化学实验,按照图1连接 好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
一化学兴趣小组在家中进行化学实验,按照图1连接 好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )| A. | NaCl是非电解质 | |
| B. | 将图2中的NaCl溶液换成液态HCl,灯泡也亮 | |
| C. | 将图2中的NaCl溶液换成SO2的水溶液,灯泡也亮,说明SO2是电解质 | |
| D. | 电解质本身不一定能导电 |