��Ŀ����
����Ŀ���������aFe2(SO4) 3��b(NH4) 2SO4��cH2O]�㷺���ڳ�����������ˮ����ҵѭ��ˮ�ľ��������ȡ�ij����������������������������ƣ��������Ϊԭ�ϣ���������¹���������ȡ������李�
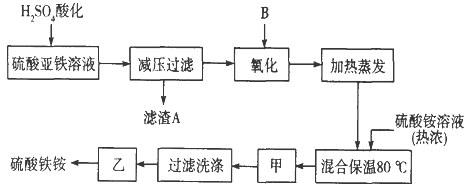
��ش��������⣺
��1������A����Ҫ�ɷ���__________________��
��2���������������ʺϵ�������B��________����Ӧ�����ӷ���ʽ__________________��
a��NaClO b��H2O2 c��KMnO4 d��K2Cr2O7
��3�������ס��ҵ����Ʒֱ��ǣ���______________����___________________��
��4�����������У�����֮��ͼ�������֮ǰ����ȡ������Һ����Fe2+�Ƿ���ȫ���������������Լ��ܷ������Ե�KMnO4��Һ��____(��ܡ����ܡ�)�����ǣ� ________________________�����������Ի�ʽ˵����
��5���������������NH4+�ķ�����________________________________________��
��6����ȡ14.00 g��Ʒ����������ˮ���Ƴ�100 mL��Һ���ֳ����ȷݣ�������һ���м�������NaOH��Һ������ϴ�ӵõ�2.14 g����������һ����Һ�м���0.05 mol Ba (NO3) 2��Һ��ǡ����ȫ��Ӧ�����������淋Ļ�ѧʽΪ______________________��
���𰸡�CaSO4bH2O2+2Fe2++2H+=2Fe3++2H2O��ȴ�ᾧ�������ɲ�����ΪH2O2��Fe2+����ʹ���Ե�KMnO4��Һ��ɫ���Թ��м���������Ʒ��NaOH������ȣ����Թܿ���ʪ��ĺ�ɫʯ����ֽ���飬������ֽ�����ɫFe2(SO4) 3��2(NH4) 2SO4��2H2O
��������
ԭ���м��������ữ������������Ƴ�������ѹ���˺�����������ɽ���������������������������������泥���80���·�Ӧ������������泥�������Ũ������ȴ�ᾧ������ϴ�ӣ��������ɹ�ɵ����������������
(1)�������ᣬ��������Һ��SO42-Ũ�ȣ���Ca2+ת��Ϊ����������CaSO4��ͬʱ����Fe2+ˮ�⣬�ʴ�Ϊ��CaSO4��
(2)Ϊ�������������ʣ�Ӧ�����������Ϊ����������ԭ������ˮ����Ӧ�����ӷ���ʽΪH2O2+2Fe2++2H+=2Fe3++2H2O���ʴ�Ϊ��b��H2O2+2Fe2++2H+=2Fe3++2H2O��
(3)��80���·�Ӧ������������泥�������Ũ������ȴ�ᾧ������ϴ�ӣ��������ɹ�ɵ�������������泥��¶Ȳ��ܹ��ߣ���ֹ�ֽ⣬�ʴ�Ϊ����ȴ�ᾧ��������ɹ��
(4)���Ը��������Һ�����Ժ�ǿ��H2O2��Fe2+����ʹ���Ե�KMnO4��Һ��ɫ��Ӧ����K3[Fe(CN)6]��Һ����������ɫ��������˵�������������ӣ��ʴ�Ϊ�����ܣ���ΪH2O2��Fe2+����ʹ���Ե�KMnO4��Һ��ɫ��
(5)����NH4+�ķ����Ǽ���ǿ�Ӧ�������ܹ�����ʹʪ��ĺ�ɫʯ����Һ���������壬�������ǰ������Ӷ�֤��ԭ��Һ��һ������NH4+���ʴ�Ϊ�����Թ��м���������Ʒ��NaOH������ȣ����Թܿ���ʪ��ĺ�ɫʯ����ֽ���飬������ֽ�����ɫ��
(6)��ȡ14.00g��Ʒ����������ˮ���ó�100mL��Һ���ֳ����ȷݣ�������һ���м�������NaOH��Һ������ϴ�ӵõ�2.14g������ӦΪFe(OH)3��n(Fe(OH)3)=![]() =0.02mol������14.00g��Ʒ�к���Fe2(SO4)30.02mol������һ����Һ�м���0.05mol Ba(NO3)2��Һ��ǡ����ȫ��Ӧ����n(SO42-)=0.05mol����n(SO42-)����Ϊ0.1mol�����(NH4)2SO4Ϊ0.1mol-0.02mol��3=0.04mol����m(H2O)=14.00g-0.02mol��400g/mol-0.04mol��132g/mol=0.72g��n(H2O)=
=0.02mol������14.00g��Ʒ�к���Fe2(SO4)30.02mol������һ����Һ�м���0.05mol Ba(NO3)2��Һ��ǡ����ȫ��Ӧ����n(SO42-)=0.05mol����n(SO42-)����Ϊ0.1mol�����(NH4)2SO4Ϊ0.1mol-0.02mol��3=0.04mol����m(H2O)=14.00g-0.02mol��400g/mol-0.04mol��132g/mol=0.72g��n(H2O)=![]() =0.04mol��n(Fe2(SO4)3)��n((NH4)2SO4)��n(H2O)=0.02��0.04��0.04=1��2��2�����Ի�ѧʽΪFe2(SO4)32(NH4)2SO42H2O���ʴ�Ϊ��Fe2(SO4)32(NH4)2SO42H2O��
=0.04mol��n(Fe2(SO4)3)��n((NH4)2SO4)��n(H2O)=0.02��0.04��0.04=1��2��2�����Ի�ѧʽΪFe2(SO4)32(NH4)2SO42H2O���ʴ�Ϊ��Fe2(SO4)32(NH4)2SO42H2O��

 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д� ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д�