题目内容
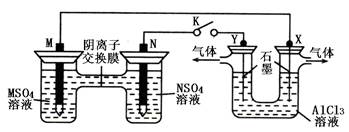
在下列装置中,MSO4和NSO4是两种常见金属的易溶盐。当K闭合时,SO42—从右到左通过交换膜移向M极,下列分析正确的是

| A.溶液中c(M2+)减小 |
| B.N的电极反应式:N=N2++2e— |
| C.X电极上有H2产生,发生还原反应 |
| D.反应过程中Y电极周围生成白色胶状沉淀 |
C
试题分析:A、当K闭合时,由图可知,左侧为原电池,右侧为电解池装置,SO42—从右到左通过交换膜移向M极,说明M极是原电池的负极,N是原电池的正极;M的活动性大于 N,原电池的总反应是M置换N,所以溶液中c(N2+)减小,错误;B、N 是原电池的正极,发生还原反应,N2+得电子生成N,电极反应式为N2++2e—=N,错误;C、右侧为电解池装置,X与负极相连,是电解池的阴极,发生还原反应,阳离子放电,所以是溶液中的氢离子放电生成氢气,正确;D、X极产生氢气,导致氢氧根离子浓度增大,所以氢氧根离子与溶液中的铝离子结合生成氢氧化铝的胶状沉淀,错误,答案选C。

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
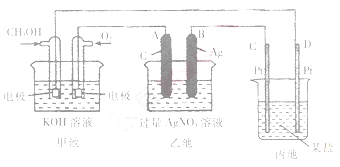
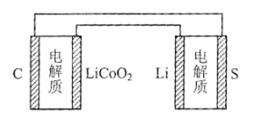
 C+LiCoO2锂硫电池的总反应为:2Li+S
C+LiCoO2锂硫电池的总反应为:2Li+S