题目内容
12.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )| A. | 2mol/L NaCl溶液中含有Na+个数为2NA | |
| B. | 常温常压下,80g NH4NO3中含有氮原子数是NA | |
| C. | 18gNH4+中含有的电子数为10NA | |
| D. | 5.6g铁与稀硝酸反应转移的电子数目一定为0.3NA |
分析 A、溶液体积不知不能计算微粒数;
B、物质的量n=$\frac{m}{M}$,每个硝酸铵中含有2个氮原子;
C、物质的量n=$\frac{m}{M}$,1个铵根离子含有10个电子;
D、物质的量n=$\frac{m}{M}$,铁和稀硝酸反应可以生成亚铁离子,也可以生成铁离子.
解答 解:A、溶液体积不知不能计算微粒数,故A错误;
B、物质的量n=$\frac{m}{M}$=$\frac{80g}{80g/mol}$=1mol,每个硝酸铵中含有2个氮原子,80g NH4NO3中含有氮原子数是2NA,故B错误;
C、物质的量n=$\frac{m}{M}$=$\frac{18g}{18g/mol}$=1mol,1个铵根离子含有10个电子,则1mol铵根离子中含电子数为10NA,故C正确;
D、物质的量n=$\frac{m}{M}$=$\frac{5.6g}{56g/mol}$=0.1mol,铁和稀硝酸反应可以生成亚铁离子,也可以生成铁离子,电子转移为0.2NA或为0.3NA,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是物质的量和微粒数的计算应用,掌握微粒结构特征和氧化还原反应产物分析是解题关键,题目较简单.

练习册系列答案
相关题目
18.迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图.下列叙述正确的是( )
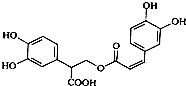

| A. | 迷迭香酸属于芳香烃 | |
| B. | 1mol迷迭香酸最多能和含6mol H2发生加成反应 | |
| C. | 迷迭香酸可以发生水解反应、消去反应和酯化反应 | |
| D. | 1mol迷迭香酸最多能和含6mol NaOH的水溶液完全反应 |
20.下列叙述中正确的是( )
| A. | 化学反应中物质变化的实质是旧化学键的断裂和新化学键的形成 | |
| B. | 离子化合物中一定有金属元素和非金属元素 | |
| C. | 全部由非金属元素形成的化合物一定是共价化合物 | |
| D. | 共价化合物中各原子都一定满足最外层8电子稳定结构 |
7.下列过程吸收能量的是( )
| A. | 钠与水反应 | B. | H+H→H2 | C. | 石灰石分解 | D. | 酸碱中和 |
1.在指定环境中,下列各组离子一定能够大量共存的是( )
| A. | 在pH=1的无色溶液中:SO42-、Cu2+、Na+、Cl- | |
| B. | 使pH试纸呈红色的溶液中:Fe2+、NO3-、SO42-、Na+ | |
| C. | 加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42- | |
| D. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1013的溶液中:NH4+、Ca2+、C1-、K+ |
2.下列试剂保存方法错误的是( )
| A. | 少量白磷保存在水里 | |
| B. | 钠保存在煤油里 | |
| C. | 液溴保存在棕色玻璃瓶里且覆盖一层水 | |
| D. | 装氢氟酸的玻璃瓶用橡皮塞 |
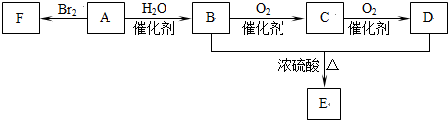
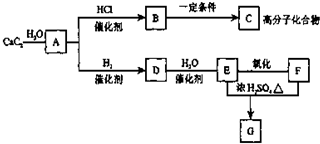 根据如图,回答问题.
根据如图,回答问题. ,GCH3COOCH2CH3
,GCH3COOCH2CH3