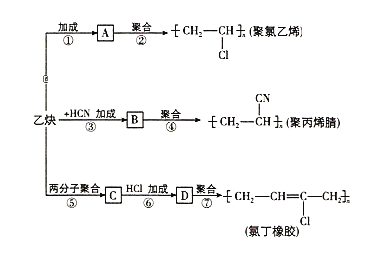
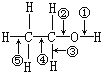
题目内容
【题目】根据下列实验现象,所得结论正确的是
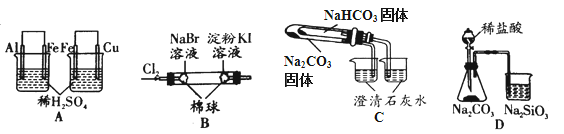
实验 | 实验现象 | 结论 |
A | 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 氧化性:Al3+>Fe2+>Cu2+ |
B | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
C | 右烧杯中澄清石灰水变浑浊,左边烧杯中无明显变化 | 热稳定性:Na2CO3>NaHCO3 |
D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
A.AB.BC.CD.D
【答案】C
【解析】
A.电解质为硫酸,活泼金属作负极,由现象可知金属性Al>Fe>Cu,即还原性Al>Fe>Cu,则氧化性Al3+<Fe2+<Cu2+,故A错误;
B.氯气可分别氧化NaBr、KI,不能比较Br2、I2的氧化性,故B错误;
C.碳酸氢钠加热分解生成碳酸钠、二氧化碳,则右烧杯中澄清石灰水变浑浊,左边烧杯中无明显变化,能够说明热稳定性:Na2CO3>NaHCO3,故C正确;
D.盐酸为无氧酸,且盐酸挥发,盐酸也能与硅酸钠反应生成白色沉淀,不能比较非金属性,故D错误;
故选C。

【题目】硼酸三丁酯的结构简式为B(OCH2CH2CH2CH3)3,常温常压下为略带香味的油状液体,是一种重要的含硼有机物,主要用作有机溶剂、脱水剂和催化剂,其一种实验室制备的原理为H3BO3+3CH3CH2CH2CH2OH![]() B(OCH2CH2CH2CH3)+3H2O,装置如图所示(夹持装置及微波加热装置已略去):
B(OCH2CH2CH2CH3)+3H2O,装置如图所示(夹持装置及微波加热装置已略去):

实验步骤如下:
Ⅰ.向微波专用圆底烧瓶中加入磁力搅拌子,并加入6.2 g硼酸(H3BO3)和47.4 mL正丁醇(CH3CH2CH2CH2OH)以及1.0 g NaHSO4H2O;
Ⅱ.微波加热:60℃下2 min,80℃下2 min,90℃下5 min,100℃下2 min,118℃下2 min;回流分水;
Ⅲ.待反应结束后,蒸馏得产品20.2 g。
已知:正丁醇的密度为0.81 g.cm-3。
请回答下列问题:
(1)分水器使用前需检查 ___,分水器的作用是 ___(任写一条)。
(2)图中仪器X的名称为 ___,其进水口应为____(填“a”或“b”)口。
(3)为了提高转化率,常用带水剂把生成的水从反应体系中分离出。分别以下列四种物质作为制备硼酸三丁酯的带水剂,结果如表所示,该实验选择正丁醇作带水剂,优点是____。
带水剂种类 | 甲苯 | 苯 | 环己烷 | 正丁醇 |
产率/% | 78.2 | 83.4 | 80.4 | 80.5 |
(4)步骤II中需要在不同温度下进行加热,并控制好时间,加热方式采用微波加热的优点是 ___;实验过程中发现,随着微波加热时间延长,硼酸三丁酯的产率增加,但当加热时间超过13 min后,产率增加幅度明显减小,造成此现象可能的原因是___。
(5)蒸馏装置中仪器的选择和安装均正确的是____(填选项字母)。
A. 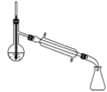 B.
B. 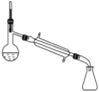 C.
C.  D.
D. 
(6)本实验中硼酸三丁酯的产率为____(保留三位有效数字)。