题目内容
12.某溶液中含有Cl-、K+、H+、SO42-,组成该溶液的化合物最多有( )| A. | 2种 | B. | 3 种 | C. | 5种 | D. | 6种 |
分析 某溶液中含有Cl-、K+、H+、SO42-,对应的溶质都为强电解质,可完全电离,以此解答.
解答 解:某溶液中含有Cl-、K+、H+、SO42-,可能含有K2SO4、KCl、HCl、H2SO4、KHSO4五种溶质,
故选C.
点评 本题考查强弱电解质在水溶液中的存在形式,侧重于电解质的电离的考查,较为基础,学生容易忽略硫酸氢盐,在水溶液中完全电离.

练习册系列答案
相关题目
2.将磷肥生产中形成的副产物石膏(CaSO4•2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义.以下是石膏转化为硫酸钾和氯化钙的某工艺流程示意图.
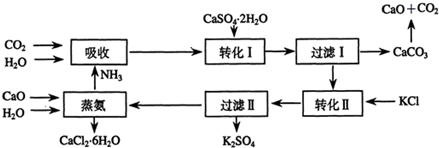
(1)在这个工艺中,有很多粒子都具有相同的电子数.
写出该工艺中具有相同电子数的四种粒子的化学式:NH3、H2O、NH4+、OH-、H3O+五种的任意四种.
(2)1919年由Langmuir提出了等电子体.原子数相同、电子数相同的粒子,互称为等电子体.A、B、C、D、E、F 是原子序数依次增大的6种位于元素周期表前20号的元素.B、C、D、E位于同周期.C是构成空气的主要元素.F与B、D都可形成XY2型离子化合物FB2、FD2,且都可与A2D(无色液体)反应放出气体.B22-与C2是等电子体,D22-与E2是等电子体.F原子的N层电子数与K层电子数相同.
①比较C、D、E对应的简单阴离子的半径(用离子符号表示)N3->O2->F-(由大到小);
②写出能证明D和E非金属性强弱的一个化学方程式2F2+2H2O=4HF+O2.
③由上述6种元素中的4种构成的离子化合物是(写出两种)NH4HCO3、(NH4)2CO3、Ca(HCO3)2、(CH3COO)2Ca其中两种,其中所含的化学键类型有离子键、共价键.
(3)①过滤Ⅱ所得滤液中大量含有的阳离子有哪些?请分别检验.(可不填满下表)
②写出此工艺的总反应方程式CaSO4•2H2O+2KCl+4H2O=K2SO4+CaCl2•6H2O.

(1)在这个工艺中,有很多粒子都具有相同的电子数.
写出该工艺中具有相同电子数的四种粒子的化学式:NH3、H2O、NH4+、OH-、H3O+五种的任意四种.
(2)1919年由Langmuir提出了等电子体.原子数相同、电子数相同的粒子,互称为等电子体.A、B、C、D、E、F 是原子序数依次增大的6种位于元素周期表前20号的元素.B、C、D、E位于同周期.C是构成空气的主要元素.F与B、D都可形成XY2型离子化合物FB2、FD2,且都可与A2D(无色液体)反应放出气体.B22-与C2是等电子体,D22-与E2是等电子体.F原子的N层电子数与K层电子数相同.
①比较C、D、E对应的简单阴离子的半径(用离子符号表示)N3->O2->F-(由大到小);
②写出能证明D和E非金属性强弱的一个化学方程式2F2+2H2O=4HF+O2.
③由上述6种元素中的4种构成的离子化合物是(写出两种)NH4HCO3、(NH4)2CO3、Ca(HCO3)2、(CH3COO)2Ca其中两种,其中所含的化学键类型有离子键、共价键.
(3)①过滤Ⅱ所得滤液中大量含有的阳离子有哪些?请分别检验.(可不填满下表)
| 所含离子 | 检验方法 |
| K+ | 取少量滤液于试管中,通过焰色反应,火焰呈紫色(透过蓝色钴玻璃) |
| NH4+ | 取少量滤液于试管中,并向其中加入NaOH微热,有刺激性气味产生(该气体可使湿润红色石蕊试纸变蓝) |
3.已知金刚石和石墨在氧气中完全燃烧的热化学方程式如下:①C(金刚石,s)+O2(g)=CO2(g)△H1=-395.41kJ/mol;②C(石墨,s)+O2(g)=CO2(g)△H2=-393.51kJ/mol.关于金刚石与石墨的转化,下列说法正确的是( )
| A. | 金刚石转化成石墨是自发进行的过程 | |
| B. | 石墨转化成金刚石是自发进行的过程 | |
| C. | 石墨和金刚石能量一样高 | |
| D. | 金刚石比石墨能量低 |
20.下列物质属于纯净物的是( )
| A. | 浮有冰块的水 | B. | 食盐水 | C. | 洁净的空气 | D. | 纯盐酸 |
7.已知:①2FeCl3+2KI═2FeCl2+2KCl+I2 ②2FeCl2+Cl2═2FeCl3,据此可判断各物质的氧化性由强到弱的顺序是( )
| A. | I2>Cl2>FeCl3 | B. | FeCl3>Cl2>I2 | C. | Cl2>I2>FeCl3 | D. | Cl2>FeCl3>I2 |
17.下列关于1.5mol 氢气的叙述中,错误的是( )
| A. | 质量是4g | B. | 标准状况下的体积约为33.6L | ||
| C. | 电子数是3mol | D. | 分子数是9.03×1023 个 |
4.用NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 0.2NA个CO分子在标准状况下的体积约是4.48 L | |
| B. | 0.1mol/L BaCl2溶液中Cl-数目是0.2 NA | |
| C. | 4℃时,22.4 L水中含有的电子数目为10NA个 | |
| D. | 使23g钠变为 Na+,需失去0.1NA个电子 |
1.下列有关阿伏加德罗常数(NA)的说法错误的是( )
| A. | 常温常压下14克CO所含的原子数目为NA个 | |
| B. | 标准状况下0.8molCCl4含有的原子数目为4NA个 | |
| C. | 任何条件下0.5mol氮气分子的分子数一定是0.5NA | |
| D. | 49克硫酸中含有的原子数目为0.5NA |