题目内容
11.用稀硫酸、氢氧化钠和铝为原料制取氢氧化铝,甲、乙、丙三学生分别用三种不同途径制备.甲.Al$\stackrel{H_{2}SO_{4}}{→}$Al2(SO4)2$\stackrel{NaOH}{→}$Al(OH)3
乙.Al$\stackrel{NaOH}{→}$NaAlO2$\stackrel{H_{2}SO_{4}}{→}$Al(OH)3
丙.
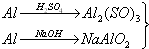 →Al(OH)3
→Al(OH)3若要制备等量的氢氧化铝,则( )
| A. | 乙消耗原料少 | B. | 三者消耗原料相同 | ||
| C. | 丙消耗原料最少 | D. | 甲、乙消耗原料相同 |
分析 若制取1molAl(OH)3,则
甲:Al~$\frac{3}{2}$H2SO4~Al(OH)3,
乙:Al~NaAlO2~$\frac{1}{2}$H2SO4~Al(OH)3,
丙:2Al+3H2SO4═Al2(SO4)3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑、Al2(SO4)3+6NaAlO2+12H2O═8Al(OH)3↓+3Na2SO4,则$\frac{3}{8}$H2SO4~Al(OH)3,以此来计算.
解答 解:若制取1molAl(OH)3,则
甲:Al~$\frac{3}{2}$H2SO4~Al(OH)3,
乙:Al~NaAlO2~$\frac{1}{2}$H2SO4~Al(OH)3,
丙:2Al+3H2SO4═Al2(SO4)3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑、Al2(SO4)3+6NaAlO2+12H2O═8Al(OH)3↓+3Na2SO4,则$\frac{3}{8}$H2SO4~Al(OH)3,则消耗硫酸的比值为$\frac{3}{2}$:$\frac{1}{2}$:$\frac{3}{8}$=12:4:3,所以消耗原料最多的是甲,最少的是丙,故选C.
点评 本题考查氢氧化铝的制备,明确制备中发生的化学反应是解答本题的关键,注意利用反应得到氢氧化铝与硫酸的关系即可解答,侧重反应的考查,题目难度中等.

练习册系列答案
相关题目
2.对下列实验操作和现象描述不正确的是( )
| A. | 过滤操作中一定要用到的玻璃仪器有烧杯、玻璃棒、漏斗 | |
| B. | 进行蒸发操作,当有大量晶体析出时,改用小火将溶液直接蒸干 | |
| C. | 用CCl4溶液将碘从水溶液中萃取出,经静置分层分液漏斗的下层为紫色 | |
| D. | 在蒸馏操作中,一般要在蒸馏瓶中加入几粒碎瓷片防止溶液暴沸 |
19.在下列分子结构中,原子的最外层电子都能满足8电子稳定结构的是( )
| A. | H2O | B. | PCl5 | C. | CCl4 | D. | CH4 |
3.苯分子中的碳碳键不是单双键交替的,不能作出这种判断的证据是( )
| A. | 苯的邻位二元取代物只有一种 | B. | 苯环中碳碳键均相同 | ||
| C. | 苯的一元取代物无同分异构体 | D. | 苯不使酸性KMnO4溶液褪色 |
20.一定温度下2L的密闭容器中发生反应:A(g)+2B(g)?xC(g)△H<0,B、C的物质的量随时间变化的关系如图所示.下列有关说法不正确的是( )
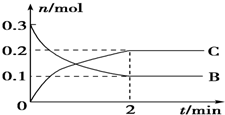

| A. | X=2 | |
| B. | 反应开始2min内,v(C)=0.05 mol•L-1•min-1 | |
| C. | 2min后,升高温度平衡向右移动 | |
| D. | 当容器内混合气体压强不再改变时,反应体系达到化学平衡状态 |
1.下列不能表明醋酸是弱电解质的是( )
| A. | 0.1mol/L的醋酸水溶液的pH值为3 | |
| B. | 常温下同浓度醋酸水溶液的导电性比盐酸弱 | |
| C. | 醋酸水溶液能使石蕊变红 | |
| D. | 醋酸稀溶液中同时存在CH3COOH和CH3COO- |