题目内容
13.下列离子方程式书写正确的是( )| A. | 硫酸铁中加入少量氨水:Fe3++3OH-═Fe(OH)3↓ | |
| B. | 电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- | |
| C. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | 将铝投入CuSO4溶液中:Al+Cu2+═Cu+Al3+ |
分析 A.一水合氨在离子反应中保留化学式;
B.电解生成NaOH、氢气、氯气;
C.碳酸钙在离子反应中保留化学式;
D.电子、电荷不守恒.
解答 解:A.硫酸铁中加入少量氨水的离子反应为Fe3++3NH3.H2O═Fe(OH)3↓+3NH4+,故A错误;
B.电解饱和食盐水的离子反应为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH-,故B正确;
C.碳酸钙与盐酸反应的离子反应为CaCO3+2H+═H2O+CO2↑+Ca2+,故C错误;
D.将铝投入CuSO4溶液中的离子反应为2Al+3Cu2+═3Cu+2Al3+,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、电解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
3.下列离子组能大量共存且溶液为无色透明的是( )
| A. | H+、K+、Cl-、NO3- | B. | Na+、H+、Cu2+、NO3- | ||
| C. | Ca2+、Na+、CO32-、Cl- | D. | Mg2+、OH-、SO42-、K+ |
8.在一定温度下的定容密闭容器中,当下列物理量不再变化时,表明反应:A(s)+2B(g)?C(g)+D(g) 已达平衡的是( )
| A. | 混合气体的压强 | B. | 混合物的总质量 | ||
| C. | B的物质的量浓度 | D. | 气体的总物质的量 |
18.现有一体积为V mL、密度为ρ g•cm-3的溶液,含有相对分子质量为M的溶质m g,其物质的量浓度为c mol•L-1,溶质的质量分数为W,下列表示式中不正确的是( )
| A. | c=$\frac{1000Wρ}{M}$ | B. | m=$\frac{VρW}{10000}$ | C. | W%=$\frac{cM}{1000ρ}$% | D. | c=$\frac{1000m}{VM}$ |
5.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
| A. | 放电时正极反应式为:3Zn-6e-+6OH-═3Zn(OH)2 | |
| B. | 充电时阳极反应式为:2FeO42-+6e-+8H2O═2Fe(OH)3+10OH- | |
| C. | 放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 | |
| D. | 放电时正极附近溶液的碱性增强 |
2.化学与生产、生活密切相关,下列说法中不正确的是( )
| A. | 食品中加入维生素或钙、硒等是为了补充食品中缺乏的营养成分 | |
| B. | 抗生素能消炎抗菌,经常大量食用对人体有益无害 | |
| C. | 使用青霉素可能产生过敏反应,用药前一定要进行皮肤敏感试验 | |
| D. | 服用麻黄碱后可明显增加运动员的兴奋程度,但对其身体有极大的副作用 |
3.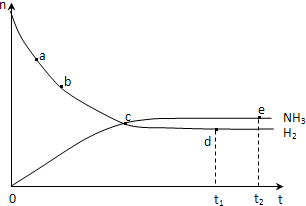 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)△H<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)△H<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)△H<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)△H<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )| A. | 点a的正反应速率比点b的小 | |
| B. | 点 c处反应达到平衡 | |
| C. | 点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样 | |
| D. | 其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值大 |