题目内容
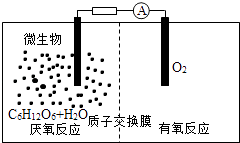
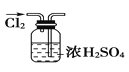
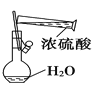
【题目】CuCl广泛应用于化工和印染等行业;某研究性学习小组拟热分解CuCl22H2O制备CuCl,并进行相关探究。已知:该小组用如图所示装置进行实验(夹持仪器略);请回答下列问题:
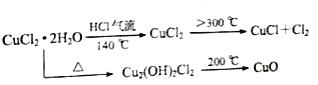
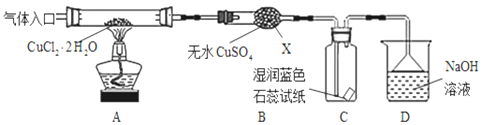
(1)仪器X的名称是_________________
(2)实验操作的先后顺序是①→______→______→______→______,_____________
①检查装置的气密性后加入药品②熄灭酒精灯,冷却 ③在“气体入口”处通干燥HCl④点燃酒精灯,加热 ⑤停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,则C中试纸的颜色变化是______
(4)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因可能是________________________________
②若杂质是CuO,则产生的原因可能是_________________________________
(5)若m克CuCl22H2O全部转化为CuO(铜元素无损耗),则固体质量减少______克。(用含m的式子表示)
【答案】 球形干燥管 )③;④;②;⑤ 石蕊试纸先逐渐变为红色,后褪色 加热时间不足或温度偏低 通入HCl的量不足 ![]()
【解析】根据已知流程可知,热分解CuCl22H2O制备CuCl,先要在HCl气流中加热得到CuCl2固体,然后高温条件下使CuCl2分解为CuCl和Cl2。Cu2+易水解,低温加热时若不通入HCl气流,则会水解生成Cu2(OH)2Cl2,高温下分解得CuO。
(1)仪器X的名称为球形干燥管,故答案为:球形干燥管;
(2)实验中有HCl气体加入,有气体生成,所以要先检验装置的气密性。在点燃酒精灯进行反应之前,要先通入气体赶走装置中的氧气和水蒸气,因为氧气会氧化CuCl,水蒸气会引起铜的水解;在HCl气流中充分加热制备CuCl;反应结束后先熄灭酒精灯,冷却后再停止HCl气流,通入氮气将装置中的Cl2全部赶入NaOH溶液中,使其被充分吸收。所以操作顺序为:③;④;②;⑤。
故答案为:③;④;②;⑤
(3)B中有白色变为蓝色,说明有水生成,产物中还有Cl2,所以C中石蕊试纸先逐渐变为红色,后褪色。
故答案为:石蕊试纸先逐渐变为红色,后褪色;
(4)①杂质是CuCl2,说明“![]() ”进行不够彻底,即CuCl2没有反应完全。可能原因是加热时间不足或温度偏低;
”进行不够彻底,即CuCl2没有反应完全。可能原因是加热时间不足或温度偏低;
故答案为:加热时间不足或温度偏低
②杂质是CuO,说明在加热过程中部分晶体水解生成Cu2(OH)2Cl2,然后分解得到了CuO,或装置中有氧气,使CuCl被氧化。可能原因为:可能是没有在HCl的氛围中加热或者未等试管冷却就停止通入HCl气体。
故答案为:通入HCl的量不足。
(5)根据关系式: CuCl22H2O~CuO,若铜没有损耗,则二者的物质的量相等,所以固体质量的减少量=m(CuCl22H2O)-m(CuO)=m-![]() =
=![]() .
.
故答案为: ![]() 。
。