题目内容
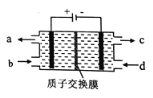
【题目】用Pt作电极电解MgCl2溶液,下列关于电解装置正确的是( )
A. 总反应式:Mg+2H2O= Mg(OH) 2↓+H2↑
B. 负极反应式:Mg2+-2e-= Mg
C. 总反应式:Mg+2H2O= Mg(OH) 2+H2↑
D. 阴极电极反应式:2H++2e-= H2↑
【答案】D
【解析】用Pt作电极电解MgCl2溶液,阳极氯离子放电,阴极氢离子放电,据此解答。
A. 用Pt作电极电解MgCl2溶液,阳极氯离子放电:2Cl――2e-=Cl2↑,阴极氢离子放电:2H++2e-=H2↑,因此总反应式:MgCl2+2H2O![]() Mg(OH)2↓+H2↑+Cl2↑,A错误;
Mg(OH)2↓+H2↑+Cl2↑,A错误;
B. 电解池中电极名称是阴阳极,不是正负极,镁离子不放电,B错误;
C. MgCl2+2H2O![]() Mg(OH)2↓+H2↑+Cl2↑,C错误;
Mg(OH)2↓+H2↑+Cl2↑,C错误;
D. 阴极电极反应式:2H++2e-=H2↑,D正确。
答案选D。

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目