题目内容
8.已知反应X+Y═M+N为放热反应,下列有关说法正确的是( )| A. | X的能量一定高于M | |
| B. | Y的能量一定高于N | |
| C. | X和Y的总能量一定高于M和N的总能量 | |
| D. | 因该反应为放热反应,所以一定不必加热就可 |
分析 当反应物的总能量大于生成物的总能量时则为放热反应,反应吸放热与反应条件无必然的联系.
解答 解:A.X和Y的总能量一定高于M和N的总能量,X的能量不一定高于M,故A错误;
B.X和Y的总能量一定高于M和N的总能量,Y的能量不一定高于N,故B错误;
C.反应X+Y=M+N为放热反应,X和Y的总能量一定高于M和N的总能量,故C正确;
D.该反应为放热反应,但引发反应时可能需要加热,故D错误.
故选C.
点评 本题考查学生放热反应的原因,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
18.下列各醇中,能发生消去反应,且生成的烯烃只有一种的( )
| A. | CH3CH2CH(OH)CH3 | B. | CH3OH | C. | 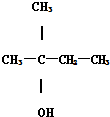 | D. | 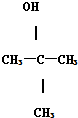 |
16.某氢氧燃料电池是用金属铂作电极,以KOH溶液作电解质溶液,从两极分别通入H2和O2.下列对该燃料电池的叙述中正确的是( )
| A. | 负极的电极反应式为:H2-2e-+2OH-═2H2O | |
| B. | H2应从负极通入,发生还原反应 | |
| C. | 标准状况下,通入5.6 L O2并完全反应后,有0.50 mol电子转移 | |
| D. | 放电一段时间后,通入O2的电极附近溶液的pH降低 |
3.如图是酸性氢氧燃料电池构造示意图.关于该电池的说法不正确的是( )
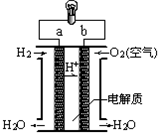

| A. | a极是负极 | |
| B. | 电流由b通过灯泡流向a | |
| C. | 正极的电极反应是:O2+2H2O+4e-═4OH- | |
| D. | 氢氧燃料电池是环保电池 |
13.同一周期中,X、Y、Z三种元素,其气态氢化物稳定性按X、Y、Z的顺序不断增强,下列说法正确的是( )
| A. | 非金属性X>Y>Z | |
| B. | 原子半径X>Y>Z | |
| C. | 它们最高价氧化物水化物的酸性按X、Y、Z顺序增强 | |
| D. | 气态氢化物的还原性按X、Y、Z顺序增强 |
20.钾的金属活动性比钠强,根本原因是( )
| A. | 钾的密度比钠的小 | B. | 加热时,钾比钠更易气化 | ||
| C. | 钾与水反应比钠与水反应更剧烈 | D. | 钾原子的电子层比钠原子多一层 |
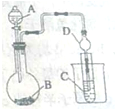 某化学兴趣小组为探究元索性质的递变规律,设计了如下系列实验.
某化学兴趣小组为探究元索性质的递变规律,设计了如下系列实验.