题目内容
【题目】(1)在25 ℃、101 kPa的条件下,请回答下列有关问题:
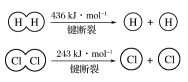
①由H+H→H2,当形成1 mol H—H键时,要________(填“吸收”或“放出”,下同)436 kJ的能量;由Cl2→Cl+Cl,当断裂1 mol Cl—Cl键时,要________243 kJ的能量。
②对于反应H2(g)+Cl2(g)=2HCl(g),测得生成2 molHCl(g)时,反应过程中放出183 kJ的热量,则断开 1 mol H—Cl 键所需的能量是________kJ。
③有两个反应:a.H2(g)+Cl2(g)![]() 2HCl(g),b.H2(g)+Cl2(g)
2HCl(g),b.H2(g)+Cl2(g)![]() 2HCl(g)。这两个反应中,相同物质的量的H2(g)、Cl2(g)反应生成相同质量的HCl(g)时,放出的能量________(填“相等”或“不相等”)。
2HCl(g)。这两个反应中,相同物质的量的H2(g)、Cl2(g)反应生成相同质量的HCl(g)时,放出的能量________(填“相等”或“不相等”)。
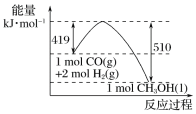
(2)①根据图示的能量转化关系判断,生成16 g CH3OH(l)________(填“吸收”或“放出”) ________kJ能量。
②1mol CO(g)的总键能_______(填“>”、“=”或“<”)1mol CH3OH(l)的总键能
【答案】放出 吸收 431 相等 放出 45.5 <
【解析】
断裂共价键时需要吸收热量,形成共价键时能够放出热量,化学反应的热效应等于反应物的总键能减去生成物的总键能,也等于生成物的总能量减去反应物的总能量,由此关系,也可求出反应物或生成物中某物质的能量或键能;对于一个化学反应,当反应物和生成物确定,化学反应的热效应也就确定,但与反应的条件无关。
(1)①形成共价键时,会放出热量,断裂共价键时,需吸收热量。从图中可以看出,当形成1 mol H-H键时,要放出436 kJ的能量;当断裂1 mol Cl-Cl键时,要吸收243 kJ的能量。
②设H-Cl 键能为x,则436kJ+243kJ-2x= -183kJ,x=431kJ,则断开 1 mol H-Cl 键所需的能量是431kJ。
③对于同一反应,当反应物的用量相同时,条件不影响反应的热效应,则两个反应:a.H2(g)+Cl2(g)![]() 2HCl(g),b.H2(g)+Cl2(g)
2HCl(g),b.H2(g)+Cl2(g)![]() 2HCl(g),相同物质的量的H2(g)、Cl2(g)反应生成相同质量的HCl(g)时,放出的能量相等。答案为:放出;吸收;431;相等;
2HCl(g),相同物质的量的H2(g)、Cl2(g)反应生成相同质量的HCl(g)时,放出的能量相等。答案为:放出;吸收;431;相等;
(2)①由图中可知,1molCO(g)与2molH2(g)完全反应生成1molCH3OH(l),放热91kJ,则生成16 g CH3OH(l)(物质的量为0.5mol),放出91kJ/mol×0.5mol=45.5kJ能量。
②由图可知,反应物的总键能-生成物的总键能= -91kJ,即1mol CO(g)的总键能+2×436kJ-1mol CH3OH(l)的总键能= -91kJ,则1mol CO(g)的总键能-1mol CH3OH(l)的总键能= -91kJ-2×436kJ<0,所以1mol CO(g)的总键能<1mol CH3OH(l)的总键能。答案为:放出;45.5;<。