题目内容
t℃时CuSO4的溶解度是S g,其饱和溶液密度d g.cm-3、物质的量浓度为c mol.L-1.向足量饱和溶液中加入m g无水CuSO4或蒸发掉n g水后恢复t℃,均能获得W g胆矾晶体,下列关系式正确的是( )
A、c=
| ||
B、S=
| ||
C、m=
| ||
D、W=
|
考点:物质的量浓度的相关计算
专题:计算题
分析:A.根据c=
计算,根据溶解度计算饱和溶液的质量分数;
B.饱和溶液蒸发掉ng水恢复到t℃时,获得Wg CuSO4?5H2O晶体,故Wg晶体再加入(蒸发掉的)n g水时,Wg胆矾晶体就可恰好溶解恢复到原饱和溶液,即n g水与Wg CuSO4?5H2O构成饱和溶液,据此计算;
C.向足量饱和溶液中加入m g无水CuSO4或蒸发掉n g水后恢复t℃,均能获得W g胆矾晶体,由于硫酸铜能与水反应而使饱和溶液硫酸铜溶液因减少水而析出晶体,因此可判断加入m g无水CuSO4相当于蒸发掉n g水,即蒸发的n g水中溶解有m g的硫酸铜;
D.析出的硫酸铜晶体质量等于加入mg硫酸铜质量与饱和溶液减少的质量,根据化学式计算硫酸铜、结晶水的质量,进而计算结晶水溶解硫酸铜的质量,结合溶解度s计算.
| 1000ρw |
| M |
B.饱和溶液蒸发掉ng水恢复到t℃时,获得Wg CuSO4?5H2O晶体,故Wg晶体再加入(蒸发掉的)n g水时,Wg胆矾晶体就可恰好溶解恢复到原饱和溶液,即n g水与Wg CuSO4?5H2O构成饱和溶液,据此计算;
C.向足量饱和溶液中加入m g无水CuSO4或蒸发掉n g水后恢复t℃,均能获得W g胆矾晶体,由于硫酸铜能与水反应而使饱和溶液硫酸铜溶液因减少水而析出晶体,因此可判断加入m g无水CuSO4相当于蒸发掉n g水,即蒸发的n g水中溶解有m g的硫酸铜;
D.析出的硫酸铜晶体质量等于加入mg硫酸铜质量与饱和溶液减少的质量,根据化学式计算硫酸铜、结晶水的质量,进而计算结晶水溶解硫酸铜的质量,结合溶解度s计算.
解答:
解:A.t℃时CuSO4的溶解度是S g,则饱和溶液的质量分数为
,根据c=
可知该溶液物质的量浓度=
mol/L=
mol?L-1,故A错误;
B.饱和溶液蒸发掉ng水恢复到t℃时,获得Wg CuSO4?5H2O晶体,逆向思维即再加入(蒸发掉的)n g水时,Wg胆矾晶体就可恰好溶解恢复到原饱和溶液,即n g水与Wg CuSO4?5H2O构成饱和溶液,饱和溶液中溶质质量=Wg×
×100%,溶液的质量=n+W,此时硫酸铜的溶解度S=
×100g=
g,故B错误;
C.加入m g无水CuSO4或蒸发掉n g水后恢复到t℃,均能获得W g胆矾晶体说明n g水后中溶解m g无水CuSO4恰好成饱和溶液,此时硫酸铜溶解度S=
×100g,则m=
g;故C正确;
D.加入m g的无水CuSO4与饱和溶液中的水反应而使饱和溶液因水减少而析出晶体,W g硫酸铜晶体中所含结晶水质量=W g×
×100%、所含硫酸铜的质量=W g×
×100%,而其中(W g×
×100%-m)g硫酸铜完全溶解于W g×
×100%g水恰好成为饱和溶液,则
=
,则析出晶体质量W=
g,故D错误;
故选C.
| s |
| 100+s |
| 1000ρw |
| M |
1000×ρ×
| ||
| 160 |
| 1000dS |
| 160(100+S) |
B.饱和溶液蒸发掉ng水恢复到t℃时,获得Wg CuSO4?5H2O晶体,逆向思维即再加入(蒸发掉的)n g水时,Wg胆矾晶体就可恰好溶解恢复到原饱和溶液,即n g水与Wg CuSO4?5H2O构成饱和溶液,饱和溶液中溶质质量=Wg×
| 160 |
| 250 |
Wg×
| ||
n+W-W×
|
| 1600W |
| 25n+9W |
C.加入m g无水CuSO4或蒸发掉n g水后恢复到t℃,均能获得W g胆矾晶体说明n g水后中溶解m g无水CuSO4恰好成饱和溶液,此时硫酸铜溶解度S=
| m |
| n |
| nS |
| 100 |
D.加入m g的无水CuSO4与饱和溶液中的水反应而使饱和溶液因水减少而析出晶体,W g硫酸铜晶体中所含结晶水质量=W g×
| 90 |
| 250 |
| 160 |
| 250 |
| 160 |
| 250 |
| 90 |
| 250 |
| S |
| 100 |
W×
| ||
W×
|
| 2500m |
| 1600-9S |
故选C.
点评:本题考查溶液浓度有关计算,涉及质量分数、溶解度、物质的量浓度,属于字母型计算,题目已知条件甚多,要求学生综合分析利用,注意理解“mg无水CuSO4与ng水恰好能够成饱和溶液”及“析出的硫酸铜晶体质量等于加入mg硫酸铜质量与饱和溶液减少的质量”,难度较大.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
“纳米材料”是当今材料科学研究的前沿,1纳米(nm)=10-9m,其研究成果广泛应用于催化及军事科学中,“纳米材料”是指直径以几纳米到几十纳米的材料,如将“纳米材料”分散到液体分散剂中,所得混合物可能具有的性质是( )
| A、具有丁达尔效应 |
| B、分散质粒子不能透过滤纸 |
| C、分散质很快就沉降下来 |
| D、所得分散系是溶液 |
在如图装置中,a为Fe,b为碳棒,关于此装置的各种叙述正确的是( )


| A、a电极上有气体放出,b电极上无气泡,溶液pH变大 |
| B、a是正极,b是负极 |
| C、导线中有电子流动,外电路中,电子从a极到b极 |
| D、a极上发生了还原反应 |
下列反应中硝酸既表现出了强氧化性又表现了酸性的是( )
| A、氧化铁与硝酸反应 |
| B、氢氧化铝与硝酸反应 |
| C、木炭粉与浓硝酸反应 |
| D、铜与硝酸反应 |
铅蓄电池在日常生活中有着广泛的应用,它的电池反应为Pb+PbO2+2H2SO4═2PbSO4+2H2O,下列说法正确的是( )
| A、正极反应为:Pb+SO42--2e-═PbSO4 |
| B、负极反应为:PbO2+SO42-+4H++2e-═PbSO4+2H2O |
| C、随着电池的工作,电解质溶液中H2SO4的浓度逐渐降低 |
| D、随着电池的工作,负极区的pH减小 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,23g NO2和N2O4的混合气体一定含有NA个氧原子 |
| B、1L 0.1mol/L NaHSO4溶液中含有0.1NA个HSO4- |
| C、将0.1mol FeCl3溶于沸水制成胶体,其中含有的胶体粒子数目为0.1NA |
| D、0.1mol Na2O2固体与足量的H2O充分反应,转移0.2NA个电子 |
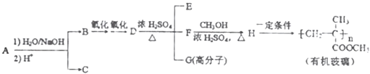
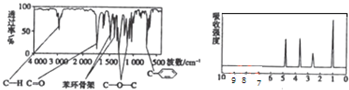
 根据氧化还原反应:Zn(s)+2Ag+(aq)═Zn2+(aq)+2Ag(s),试设计一个简单的原电池.
根据氧化还原反应:Zn(s)+2Ag+(aq)═Zn2+(aq)+2Ag(s),试设计一个简单的原电池.