题目内容
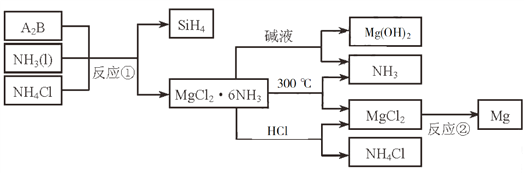
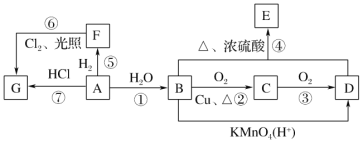
【题目】已知A是用来衡量一个国家石油化工发展水平的标志性物质,A、B、C、D、E、F、G均为有机物,他们之间有如图所示的转化关系,请回答下列问题:
(1)A中官能团的名称为___,B中官能团的电子式为__。
(2)在F的同系物中最简单的有机物的空间构型为__。
(3)写出与F互为同系物的含5个碳原子的有机物的所有同分异构体中,其中一氯代物种类最少的同分异构体的结构简式:___。
(4)写出下列编号对应反应的化学方程式,并注明反应类型:
②___,___;
④___,___。
【答案】碳碳双键 ![]() 正四面体形 C(CH3)4 2CH3CH2OH+O2
正四面体形 C(CH3)4 2CH3CH2OH+O2![]() 2CH3CHO+2H2O 氧化反应 CH3CH2OH+CH3COOH
2CH3CHO+2H2O 氧化反应 CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O 取代反应(或酯化反应)
CH3COOCH2CH3+H2O 取代反应(或酯化反应)
【解析】
已知A是用来衡量一个国家石油化工发展水平的标志性物质,则A为乙烯,A与水反应生成B(乙醇),B催化氧化生成C(乙醛),乙醛催化氧化生成D(乙酸),乙醇和乙酸反应生成E(乙酸乙酯),A和氢气反应生成F(乙烷),A和HCl反应生成氯乙烷。
⑴A是乙烯,含中官能团的名称为碳碳双键,B为乙醇,官能团为羟基,其电子式为![]() ;故答案为:碳碳双键;
;故答案为:碳碳双键;![]() 。
。
⑵F为乙烷,其同系物中最简单的有机物是甲烷,甲烷的空间构型为整四面体形,故答案为:正四面体形。
⑶F为乙烷,与乙烷互为同系物的含5个碳原子的有机物的分子式为C5H12,其同分异构体为正戊烷、异戊烷、新戊烷,一氯代物种类最少的同分异构体为新戊烷,其结构简式为C(CH3)4;故答案为:C(CH3)4。
⑷②是乙醇的催化氧化反应生成乙醛,反应方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O,反应类型为氧化反应;故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O,反应类型为氧化反应;故答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;氧化反应。
2CH3CHO+2H2O;氧化反应。
④是乙醇和乙酸发生酯化反应生成乙酸乙酯,反应方程式为:CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O,反应类型为取代反应(或酯化反应);故答案为:CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O,反应类型为取代反应(或酯化反应);故答案为:CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O;取代反应(或酯化反应)。
CH3COOCH2CH3+H2O;取代反应(或酯化反应)。

【题目】结合所学内容,回答下列问题:
Ⅰ.某同学进行影响草酸与酸性高锰酸钾溶液反应速率因素的研究。室温下,两支试管分别编号①和②,实验数据如下:
实验序号 | ① | ② | ③ |
加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的MnSO4固体 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的Na2SO4固体 |
褪色时间/s | 116 | 6 |
试管①中KMnO4溶液褪色的速率开始十分缓慢,一段时间后突然加快。
请回答:
(1)草酸与酸性高锰酸钾的反应的离子方程式为:__________________________________
(2)实验①②结论是___________________________________________________________。
(3)实验②选用MnSO4固体而不是MnCl2固体的原因是____________________________。
(4)该同学为使实验更加严密,在试管③中做了如下实验,请预测褪色时间约为________。
Ⅱ.滴定法是一种重要的定量分析方法,应用范围很广。某地市场上销售的一种食用精制盐包装袋上有如下部分说明:
产品等级 | 一级 |
配料 | 食盐、碘酸钾(KIO3)、抗结剂 |
碘含量(以I计) | 20~50 mg·kg-1 |
已知:IO3-+5I-+6H+ = 3I2+3H2O,I2+2S2O32- = 2I-+S4O62-某学生拟测定食用精制盐的碘含量,其步骤为
a.准确称取W g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.加入指示剂,逐滴加入物质的量浓度为2.0×10-3 mol·L-1的Na2S2O3溶液10.0 mL,恰好反应完全
(5)c中加入的指示剂可选用_________,恰好完全反应时的现象是_______________。
(6))若操作b在空气中振荡时间过长,则最终测定的测定食用精制盐中的的碘含量会__________(填“偏高”、“偏低”或“没有影响”)。
(7)根据以上实验和包装说明,算得所测食用精制盐的碘含量是(以含W的代数式表示)_____mg·kg-1(计算结果保留整数即可)。