题目内容
【题目】下列说法错误的是( )
A. 用托盘天平称取3.2 g NaCl固体
B. 过滤和向容量瓶转移液体时,玻璃棒的作用相同
C. 容量瓶使用前应洗涤、干燥、检漏
D. 定容时,加水不慎超过刻度线,只能重新配置
【答案】C
【解析】
A. 托盘天平的精确度为0.1g,因此可以用托盘天平称取3.2 g NaCl固体,A项正确;
B. 过滤和向容量瓶转移液体时,玻璃棒的作用均为引流,作用相同,B项正确;
C. 容量瓶使用前应先检漏,再进行洗涤,无需干燥,C项错误;
D. 定容时,加水不慎超过刻度线,所配置的溶液变稀,只能重新配置,D项正确;
答案应选C。

 阅读快车系列答案
阅读快车系列答案【题目】某化学兴趣小组为探究浓硫酸的性质,设计了如下图所示的装置进行实验。
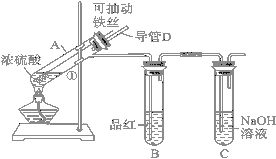
(1)用“可抽动的铁丝”代替“直接投入铁片”的优点是________________。
(2)说明SO2气体产生的实验现象是___________;装置C的作用是______________。
(3)反应一段时间后,他们对试管A中溶液的金属离子进行探究,请完成相关试题:
① 提出假设: 假设1:只含有Fe3+;
假设2:只含有Fe2+;
假设3:既有Fe2+,又有Fe3+。
② 请设计实验方案验证假设3。
限选试剂:稀硫酸、KMnO4溶液、KSCN溶液、NaOH溶液、H2O2溶液。
实验步骤 | 预期现象 |
步骤一:用胶头滴管取出A试管中的溶液,用水稀释后,并分装在试管Ⅰ、Ⅱ中备用 |
|
步骤二:检验Fe3+,往试管Ⅰ中,_____________ | _________________________ |
步骤三:检验Fe2+,往试管Ⅱ中,______________ | _________________________ |
(4)已知C+2H2SO4(浓)![]() 2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的_____
2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的_____
A.脱水性 B.强氧化性 C.吸水性
若要验证反应产物中同时混有SO2气体和CO2气体,可选择以下试剂进行实验:
NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序为_____________________(填序号)。