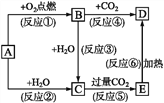
��Ŀ����
����Ŀ��ij��ѧ��ȤС��Ϊ̽��Ũ��������ʣ����������ͼ��ʾ��װ�ý���ʵ�顣
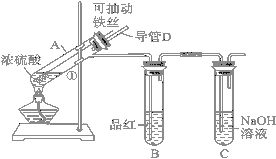
��1���á��ɳ鶯����˿�����桰ֱ��Ͷ����Ƭ�����ŵ���________________��
��2��˵��SO2���������ʵ��������___________��װ��C��������______________��
��3����Ӧһ��ʱ������Ƕ��Թ�A����Һ�Ľ������ӽ���̽���������������⣺
�� ������裺 ����1��ֻ����Fe3����
����2��ֻ����Fe2����
����3������Fe2��������Fe3����
�� �����ʵ�鷽����֤����3��
��ѡ�Լ���ϡ���ᡢKMnO4��Һ��KSCN��Һ��NaOH��Һ��H2O2��Һ��
ʵ�鲽�� | Ԥ������ |
����һ���ý�ͷ�ι�ȡ��A�Թ��е���Һ����ˮϡ�ͺ���װ���Թܢ��б��� |
|
�����������Fe3�������Թܢ��У�_____________ | _________________________ |
������������Fe2�������Թܢ��У�______________ | _________________________ |
��4����֪C��2H2SO4(Ũ)![]() 2SO2����CO2����2H2O���÷�Ӧ����Ũ�����_____
2SO2����CO2����2H2O���÷�Ӧ����Ũ�����_____
A����ˮ�ԡ� B��ǿ�����ԡ� C����ˮ��
��Ҫ��֤��Ӧ������ͬʱ����SO2�����CO2���壬��ѡ�������Լ�����ʵ�飺
NaOH��Һ ��Ʒ����Һ ����ˮ ��Ca(OH)2��Һ
ѡ������Լ��������ź�����˳��Ϊ_____________________������ţ���
���𰸡� ����ʱ���Ʒ�Ӧ�Ľ��к�ֹͣ Ʒ����ɫ ���ն����SO2���壬��ֹβ����Ⱦ�������� ���뼸��KSCN��Һ ��Һ����Ѫ��ɫ ��������KMnO4��Һ�����ȵ��뼸��ϡ���ᣩ �Ϻ�ɫ��dz������ B �ڢۢڢ�
����������1���ڼ��ȵ������£�����˿��Ũ����Ӵ�ʱ���ܷ�Ӧ�������ϳ鶯��˿ʱ����˿������Ӵ�����Ӧֹͣ�������á��ɳ鶯����˿�����ŵ��ǿ���ʱ���Ʒ�Ӧ�Ľ��к�ֹͣ����2��SO2����Ư���ԣ�Ʒ����Һ�ܱ���������Ư�ף�����Ʒ����Һ��֤SO2�����ɣ�������˵����SO2���������ʵ��������Ʒ����Һ��ɫ������������ж��ԣ��ܱ������������գ����װ��C�����������ն����SO2���壬��ֹβ����Ⱦ������������3�����ʵ�鷽����֤����3������֤Fe3+��Fe2+������һ���ý�ͷ�ι�ȡA�Թ��е���Һ����ˮϡ�Ͳ���װ�Թ�I��II���ã�����������Թ�I�У��μ�������KSCN��Һ����Һ����Ѫ��ɫ����˵��ԭ��Һ�к���Fe3+�������������Թ�II�μӵ�������KMnO4��Һ��Fe2+�ܻ�ԭ����������ӣ�����Һ��ɫ����˵��ԭ��Һ�к���Fe2+����4����ӦC��2H2SO4(Ũ)![]() 2SO2����CO2����2H2O��̼���ʱ�Ũ�����������÷�Ӧ����Ũ�����ǿ�����ԣ���ѡB����Ҫ��֤��Ӧ������ͬʱ����SO2�����CO2���壬����SO2�ܸ���CO2�ļ��飬�����ȼ�����������ٳ����������������������̼���ɣ����ѡ���Լ����ź�����˳��Ϊ�ڢۢڢ���
2SO2����CO2����2H2O��̼���ʱ�Ũ�����������÷�Ӧ����Ũ�����ǿ�����ԣ���ѡB����Ҫ��֤��Ӧ������ͬʱ����SO2�����CO2���壬����SO2�ܸ���CO2�ļ��飬�����ȼ�����������ٳ����������������������̼���ɣ����ѡ���Լ����ź�����˳��Ϊ�ڢۢڢ���

����Ŀ�����������ڹ�ҵ������Ӧ�ù㷺��ij���н����٣�W����WO2��WO3��W2O5�Ļ������Ӹû�����з����WO3��W2O5����ұ�������٣���������ͼ��ʾ��
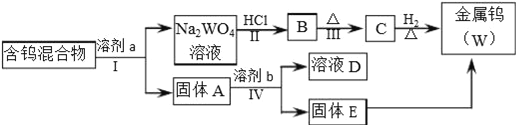
���Ķ����Ͽ�Ƭ���ش��������⣮
�����Ͽ�Ƭ��
i��WO3������NaOH��Na2CO3��Na2C2O4�������ƣ���Һ���γ������Σ�Na2WO4����W2O5�ױ�������Ҳ���ܽ���������Һ�У������ٺ�WO2������������Һ��
ii��WO3�����������ᷴӦ��
iii���ٻ������ڲ�ͬ�ܼ��еĽ�ȡ�ʼ��±�����ȡ�����ܼ��ܽ��������Է����������ּ������Ĺ��̣�����ȡ��Ϊ100%��������еĿ������ȫ���ܽ����ܼ��У���
�ܼ� | ���ʱ�䣨min�� | W2O5��%�� | WO3��%�� | WO2 | ������ |
��100g/L NaOH ��300g/LNa2CO3 ��50g/L Na2CO3 �ܱ���Na2C2O4 �ݱ���Na2C2O4����CO2�����½�ȡ�� | 25 7 30 60 120 | 72.3 76.4 100 4.2 ��0.5 | 100 100 100 100 100 | δ��� | δ��� |
��1�������͢���Ҫ���еIJ�����_______________________________________��
��2�������Ӧ�Ļ�ѧ����ʽ�ֱ���_____________��_____________��
��3��WO3�����ڽ��������Ҳ����____������ԡ��������ԡ����������NaOH��Һ��Ӧ�����ӷ���ʽ��___________________________��
��4��������ǽ�WO3���������ѡ�õ��Լ�a�Ǣݣ�������______��
��5��������ɽ�W2O5���������ѡ�õ��Լ�b��____������E�к��е�������___��D�е�������____��