题目内容
【题目】非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
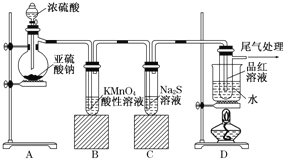
(1)若A常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是________;
②在工业生产中B气体的大量排放被雨水吸收后形成______而污染了环境。
(2)若A在常温下为气体,C是红棕色的气体.
①A、C的化学式分别是:A________;C________。
② C→D反应的化学方程式 __________________________________;该反应________(填“属于”或“不属于”)氧化还原反应。
【答案】H2SO4 酸雨 N2 NO2 3NO2+H2O=2HNO3 +NO 属于
【解析】
题中能发生连续氧化,对应的反应有硫和氮元素的转化:
(1)A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体,则A为S元素,B为SO2,C为SO3,D为H2SO4,
(2)A在空气中的主要成分,C是红棕色的气体,则A应为N2,B为NO,C为NO2,D为HNO3,结合物质的性质解答该题。
题中能发生连续氧化,对应的反应有硫和氮元素的转化:
(1)A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体,则A为S元素,B为SO2,C为SO3,D为H2SO4,
①由以上分析可知D的化学式是H2SO4,故答案为:H2SO4。
②B是二氧化硫,二氧化硫和水反应生成亚硫酸,亚硫酸不稳定易被氧化生成硫酸,硫酸溶液呈酸性,雨水中含有硫酸而形成酸雨,故答案为:酸雨。
(2)A在常温下为气体,C是红棕色的气体,则A应为N2,B为NO,C为NO2,D为HNO3,
①由以上分析可知A、C的化学式分别是N2、NO2,故答案为:N2;NO2。
②C为NO2,可与H2O反应生成HNO3和NO,反应的化学方程式为3NO2+H2O=2HNO3 +NO,该反应中N元素的化合价由+4价升高为+5价,降低为+2价,化合价发生了变化,属于氧化还原反应,故答案为:3NO2+H2O=2HNO3 +NO,属于。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案