题目内容
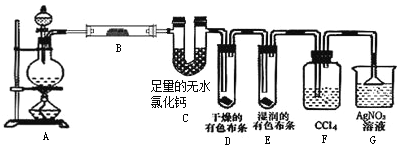
【题目】某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
(1)写出A中实验室制氯气的化学方程式________。
(2)①装置B中盛放的试剂名称为________,现象是________。
②装置D和E中出现的不同现象说明________。
③装置F的作用是________。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在装置F和装置G之间再加一个装置,该装置中应放入________(填写试剂或用品名称)。
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 无水硫酸铜 白色固体变为蓝色 氯气无漂白性,湿润的氯气有漂白性(或次氯酸有漂白性) 吸收氯气 湿润的淀粉KI试纸(或湿润的有色布条)
MnCl2+Cl2↑+2H2O 无水硫酸铜 白色固体变为蓝色 氯气无漂白性,湿润的氯气有漂白性(或次氯酸有漂白性) 吸收氯气 湿润的淀粉KI试纸(或湿润的有色布条)
【解析】
(1)实验室用二氧化锰与浓盐酸反应制备氯气;
(2)①利用无水硫酸铜遇到水变蓝性质检验氯气中是否含有水蒸气;
②依据干燥的有色布条不褪色,湿润的有色布条褪色,对比说明具有漂白性的不是氯气;
③氯气易溶于CCl4;
(3)G装置是用来检验HCl气体的,为确保实验结论的可靠性,需要排除氯气的干扰,氯气可氧化碘化钾得到单质碘,碘与淀粉变蓝,据此作答;
A.实验时用二氧化锰与浓盐酸在加热条件下反应来制备氯气,生成氯化锰、水和氯气,反应的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,
MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)①为了探究在实验室制备Cl2的过程中有水蒸气,可以在B中加入无水硫酸铜,如果固体变蓝则证明氯气中含有水蒸气,
故答案为:无水硫酸铜;白色固体变为蓝色;
②干燥的有色布条不褪色,湿润的有色布条褪色,说明具有漂白性的不是氯气,而是氯水中的次氯酸,
故答案为:氯气无漂白性,湿润的氯气有漂白性(或次氯酸有漂白性);
③氯气易溶于CCl4,所以该装置的作用是吸收氯气,
故答案为:吸收氯气;
(3)G装置用来检验HCl气体,为了确保实验结论的可靠性,应排除氯气的干扰,在F吸收氯气之后要检验氯气是否完全除去,根据氯气具有强氧化性的性质,可用湿润的淀粉KI试纸检验,其反应方程式为:Cl2+2KI=2KCl+I2,生成的碘遇淀粉变蓝,如不变色,说明已经完全除去,所以可以在F和G之间连接一个盛有湿润的淀粉碘化钾试纸的洗气瓶检验是否存在氯气,另外根据氯气的漂白性,也可在F和G之间连接一个盛有湿润的有色布条的洗气瓶,若不褪色,则证明氯气已被完全吸收,此方法也可行。
故答案为:湿润的淀粉KI试纸(或湿润的有色布条)

 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案【题目】温度为T1时,在三个容积均为1L的恒容密闭容器中仅发生反应:2NO2(g)![]() 2NO(g)+O2(g)相关数据如下表所示。下列说法错误的是( )
2NO(g)+O2(g)相关数据如下表所示。下列说法错误的是( )
容器 编号 | 物质的起始浓度 (mol·L-1) | 物质的平衡浓度 (mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A. 容器Ⅰ中发生反应的平衡常数为0.8 B. 容器Ⅱ中发生反应的起始阶段有v正>v逆
C. 达到平衡时,容器Ⅲ中![]() >1 D. 达到平衡时,容器Ⅰ与容器Ⅲ中的总压强之比为16∶17
>1 D. 达到平衡时,容器Ⅰ与容器Ⅲ中的总压强之比为16∶17
【题目】下列物质分类的正确组合是( )
分类组合 | 纯净物 | 电解质 | 酸性氧化物 | 碱性氧化物 |
A. | 漂白粉 | 氨水 | 二氧化碳 | 氧化铝 |
B. | 干冰 | 碳酸钙 | 一氧化氮 | 四氧化三铁 |
C. | CaCl2·8NH3 | 水 | 三氧化硫 | 过氧化钠 |
D. | 液氨 | 氯化氢 | 二氧化硅 | 氧化钙 |
A.AB.BC.CD.D
【题目】一定温度下,向10 mL 0.40 mol/L H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示。资料显示,反应分两步进行:
①2Fe3++ H2O2 ![]() 2Fe2++ O2↑+ 2H+,② H2O2 + 2Fe2+ + 2H+
2Fe2++ O2↑+ 2H+,② H2O2 + 2Fe2+ + 2H+ ![]() 2Fe3++2H2O,
2Fe3++2H2O,
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
反应过程中能量变化如下图所示。

下列说法不正确的是
A. 0~6 min的平均反应速率:v(H2O2) = 3.33×10-2 mol/( L·min)
B. Fe3+的作用是增大过氧化氢的分解速率
C. 反应①是吸热反应、反应②是放热反应
D. 反应2H2O2(aq) ![]() 2H2O(l) + O2(g)的△H > 0
2H2O(l) + O2(g)的△H > 0