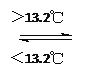题目内容
【题目】可逆反应aA(g)+bB(s) ![]() cC(g)+dD(g),在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是( )
cC(g)+dD(g),在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是( ) 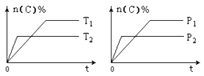
A.温度降低,化学平衡向逆反应方向移动
B.使用催化剂,C的物质的量分数增加
C.化学方程式系数a<c+d
D.平衡时再加入A,平衡向右移动,A的转化率增大
【答案】C
【解析】A、正反应为放热反应,温度降低,化学平衡向正反应方向移动,A不符合题意;
B、催化剂只改变化学反应速率,对平衡移动没有影响,C的质量分数不变,B不符合题意;
C、压强越大,平衡时C的体积分数n(C)%越小,可知正反应为气体物质的量增大的反应,即a<c+d,C符合题意;
D、平衡时再加入A,A的浓度增大,平衡向右移动,但A的转化率减小,D不符合题意;
故答案为:C可逆反应,当其他条件一定时,温度越高,反应速率越大,达到平衡所用的时间越短.由图象(1)可知T2>T1 , 温度越高,平衡时C的体积分数n(C)%越小,故此反应的正反应为放热反应;当其他条件一定时,压强越高,反应速率越大,达到平衡所用的时间越短.由图(2)可知p2>p1 , 压强越大,平衡时C的体积分数n(C)%越小,可知正反应为气体物质的量增大的反应,即a<c+d;据此分析选项。

 阅读快车系列答案
阅读快车系列答案【题目】无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点231.9℃)与Cl2反应制备SnCl4,装置如图所示。回答下列问题:

已知:①SnCl4在空气中极易水解生成SnO2·хH2O
②
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
(1)仪器A的名称是_______,其中发生反应的离子方程式是____________。
(2)点燃酒精灯前需排尽装置中的空气,否则会发生副反应,化学方程式是______、_____。
(3)试剂 B、C依次为_______,试剂B的作用是______。
(4)Cl2 和锡的反应产物有SnCl4和SnCl2,为防止产品中带入 SnCl2,可采取的措施是_______、_______。
(5)碘氧化法滴定分析产品中2价Sn(II)的含量。准确称取m g产品于锥形瓶中,用蒸馏水溶解,淀粉-KI溶液做指示剂,用c mol·L-1 碘标准溶液滴定至终点,消耗碘标准溶液V mL,计算产品中Sn(II)的含量_______(用含c、m、V的代数式表示)。