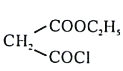题目内容
【题目】下列有关电子排布的表述正确的是( )
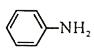
A.![]() 可表示单核8电子粒子基态时电子排布
可表示单核8电子粒子基态时电子排布
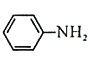
B.![]() 此图错误,违背了洪特规则
此图错误,违背了洪特规则
C.2p3表示基态氮原子的外围电子排布式
D.![]() 表示处于激发态的硼原子的电子排布图
表示处于激发态的硼原子的电子排布图
【答案】B
【解析】
A.根据洪特规则:在相同能量的轨道上,电子在排布的时候优先进入空轨道,每个轨道中的单电子自旋方向相同,所以单核8电子粒子基态时电子排布为![]() ,故A错误;
,故A错误;
B.根据洪特规则:在相同能量的轨道上,电子在排布的时候优先进入空轨道,每个轨道中的单电子自旋相同相同,则![]() 违背了洪特规则,故B正确;
违背了洪特规则,故B正确;
C.基态氮原子的外围电子排布式应为2s22p3,故C错误;
D.激发态的B原子的2p电子应跃迁到3s轨道或更高能级,2p的三个轨道能量相同,不是激发态,故D错误;
故答案为B。

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案【题目】现有部分元素的原子结构特点如表,下列叙述中正确的是( )
X | L层电子数是K层电子数的3倍 |
Y | 核外电子层数等于原子序数 |
Z | L层电子数是K层和M层电子数之和 |
W | 共用三对电子形成双原子分子,常温下为气体单质 |
A.W原子结构示意图为![]()
B.元素X和Y只能形成原子个数比为1∶2的化合物
C.元素X比元素Z的非金属性强
D.X、Y、Z、W四种元素不能形成离子化合物
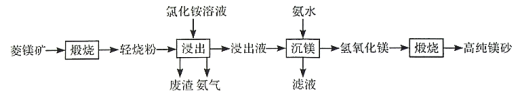
【题目】用软锰矿(主要成分为MnO2,含少量Fe3O4、Al2O3)和BaS制备高纯MnCO3的工艺流程如下:
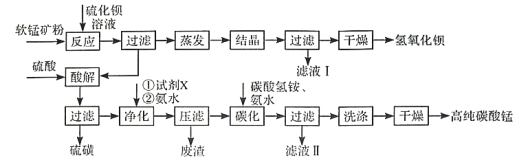
已知:MnO2是一种两性氧化物;25℃时相关物质的Ksp见下表。
物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
Ksp |
|
|
|
|
回答下列问题
(1)软锰矿预先粉碎的目的是____________,MnO2与BaS溶液反应转化为MnO的化学方程式为________。
(2)保持BaS投料量不变,随MnO2与BaS投料比增大,S的量达到最大值后无明显变化,而Ba(OH)2的量达到最大值后会减小,减小的原因是________。
(3)滤液I可循环使用,应当将其导入到________操作中(填操作单元的名称)。
(4)净化时需先加入的试剂X为________(填化学式)。再使用氨水调溶液的pH,则pH的理论最小值为_______(当溶液中某离子浓度![]() 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
(5)碳化过程中发生反应的离子方程式为______________________。