题目内容
17.已知元素周期表中第ⅡA族元素有铍、镁、钙、锶、钡、镭,钙与水反应较剧烈,下列关于锶单质的性质描述错误的是( )| A. | 将颗粒状锶单质放入水中,反应剧烈,生成大量的气体,气体燃烧且发生轻微爆炸 | |
| B. | 颗粒状锶单质与稀硫酸反应,反应现象不如钠与水反应剧烈 | |
| C. | 锶在纯氧中可以燃烧,燃烧产物与水反应生成的氢氧化物为强碱 | |
| D. | 锶在纯净氮气中可以燃烧,燃烧产物与水反应可以放出气体 |
分析 第ⅡA族元素有铍、镁、钙、锶、钡、镭,同主族元素从上到下金属性逐渐增强,金属性越强,其单质与水反应越剧烈,其最高价氧化物的水化物的碱性越强;锶在纯净氮气中可以燃烧生成氮化锶,氮化锶与水反应生成氨气,据此分析.
解答 解:A.锶的活泼性大于钙,所以与水反应更剧烈,则将颗粒状锶单质放入水中,反应剧烈,生成大量的气体,气体燃烧且发生轻微爆炸,故A正确;
B.金属的活泼性:Sr>Ca>Na,则颗粒状锶单质与稀硫酸反应,反应现象比钠与水反应剧烈,故B错误;
C.锶的最高价氧化物的水化物为强碱,则锶在纯氧中可以燃烧,燃烧产物与水反应生成的氢氧化物为强碱,故C正确;
D.锶在纯净氮气中可以燃烧生成氮化锶,氮化锶与水反应生成氨气,所以锶在氮气中燃烧产物与水反应可以放出气体,故D正确.
故选B.
点评 本题考查了元素周期律,侧重于同主族元素性质的考查,注意把握同主族元素性质的变化规律,题目难度不大.

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
5.关于给定的原电池的下列说法中,错误的是( )


| A. | 铜片作正极,锌片作负极 | |
| B. | 该电池工作时,锌失电子变为Zn2+进入溶液 | |
| C. | 该电池工作时,电子由锌片流向铜片 | |
| D. | 该电池工作时,H+在锌片上得电子被还原生成H2逸出 |
12.现代生活中,人们出行的代步工具多种多样,消耗的能量类型各不相同.自行车、电动自行车、普通汽车消耗的能量类型分别是①生物质能②核能③电能④太阳能⑤化学能( )
| A. | ①④⑤ | B. | ①③⑤ | C. | ①②③ | D. | ①③④ |
2.下列说法正确的是( )
| A. | 可通过控制溶液的pH降低氨基酸的熔点,分离不同氨基酸 | |
| B. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰钾溶液褪色 | |
| C. | 所有的糖类、油脂和蛋白质均能发生水解反应 | |
| D. | 利用二氧化碳制造全降解塑料能有效减少“白色污染” |
6.下列除杂过程中,选用试剂和方法正确的是( )
| A. | 除去乙烷中混有的乙烯,加氯气光照 | |
| B. | 除去乙烯中混有的水蒸气,通过盛有浓硫酸的洗气瓶 | |
| C. | 除去乙烷中混有水蒸气,通过碱石灰的干燥管 | |
| D. | 除去乙烯中混有的少量SO2,通过KMnO4酸性溶液后再干燥 |
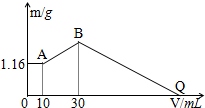 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol/LHCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示.试回答:
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol/LHCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示.试回答: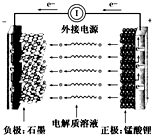 通常氢氧燃料电池有酸式和碱式两种,试回答下列问题:
通常氢氧燃料电池有酸式和碱式两种,试回答下列问题: