题目内容
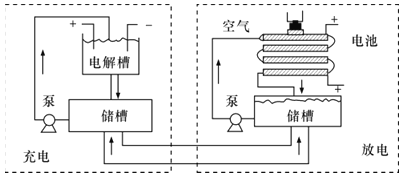
【题目】二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的绿色消毒剂,纯ClO2易分解爆炸,其一种生产工艺如下,回答下列问题:

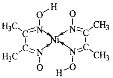
(1)气体A的名称为___________________,NCl3的电子式为_________。
(2)“电解”过程中生成的氧化产物与还原产物的物质的量之比为________。
(3)气体B能使石蕊试液显蓝色,写出NaClO2溶液和NCl3溶液在碱性条件下生成“混合气”的化学方程式____________。
(4)通常用单位质量的消毒剂得到电子的多少来衡量消毒效率的大小。C1O2和C12在消毒时自身均被还原为Cl-,则C1O2的消毒效率是Cl2的__________倍。
(5)科学家又研究出了一种新的制备C1O2的方法,反应原理如下:H2C2O4+2NaClO3+H2SO4=Na2SO4+2CO2↑+2ClO2↑+2H2O。此法提高了生产及储存、运输的安全性,原因是_____________________。若反应中转移1mol电子,则生成C1O2 ______ g。
【答案】氢气 ![]() 1:3 6NaClO2+NCl3+3H2O=6ClO2↑+NH3↑+3NaCl+3NaOH 2.63 反应过程中生成的二氧化碳起到稀释作用 67.5
1:3 6NaClO2+NCl3+3H2O=6ClO2↑+NH3↑+3NaCl+3NaOH 2.63 反应过程中生成的二氧化碳起到稀释作用 67.5
【解析】
根据工艺流程图,结合题中的信息,氯化铵溶液中加入盐酸电解的方程式为NH4Cl+2HCl![]() NCl3+3H2↑;气体B能使石蕊试液显蓝色,气体B为氨气,依据反应物、生成物可以NaClO2溶液和NCl3溶液在碱性条件下生成“混合气”的化学方程式;通常用单位质量的消毒剂得到电子的多少来衡量消毒效率的大小,故比较相同质量的C1O2和C12在消毒时自身均被还原为Cl-,转移电子的数目;
NCl3+3H2↑;气体B能使石蕊试液显蓝色,气体B为氨气,依据反应物、生成物可以NaClO2溶液和NCl3溶液在碱性条件下生成“混合气”的化学方程式;通常用单位质量的消毒剂得到电子的多少来衡量消毒效率的大小,故比较相同质量的C1O2和C12在消毒时自身均被还原为Cl-,转移电子的数目;
(1)由分析可知,气体A是H2,NCl3的电子式为![]() ;
;
(2)根据电解的化学方程式:NH4Cl+2HCl![]() NCl3+3H2↑,NCl3为氧化产物,还原产物为氢气,氧化产物与还原产物的物质的量之比为1:3;
NCl3+3H2↑,NCl3为氧化产物,还原产物为氢气,氧化产物与还原产物的物质的量之比为1:3;
(3)能使石蕊试液显蓝色的气体是氨气,根据生产工艺流程图,可写出生成“混合气”的化学方程式为6NaClO2+NCl3+3H2O=6ClO2↑+NH3↑+3NaCl+3NaOH;
(4)ClO2的消毒效率(等质量时得到电子的多少)是Cl2的![]() =2.63倍;
=2.63倍;
(5)因为ClO2易分解爆炸,生成的二氧化碳起到稀释作用,防止爆炸;分析化学方程式可知关系式:ClO2~e-,当转移1mol e-时,生成C1O2为1mol,即67.5g。

 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案