题目内容
5.下列关于工业生产的叙述中,错误的是( )| A. | 制普通玻璃的主要原料是纯碱、石灰石、石英 | |
| B. | 氨是制作氮肥、硝酸、铵盐的重要原料 | |
| C. | 将氢气和氯气混合光照生成氯化氢,溶于水制得盐酸 | |
| D. | 制造普通水泥的主要原料是黏土、石灰石 |
分析 A.根据玻璃的组成可知,制玻璃的原料主要是纯碱、石灰石和石英;
B.氨是氮肥工业及制造硝酸、铵盐、氮肥等重要原料;
C.氢气和氯气混合光照易爆炸;
D.制造普通水泥的主要原料是粘土、石灰石.
解答 解:A.普通玻璃的主要原料是纯碱、石灰石和石英,窑里加强热时,碳酸钙和二氧化硅在高温下生成硅酸钙和二氧化碳,碳酸钠和二氧化硅在高温下生成硅酸钠和二氧化碳,故A正确;
B.氨是一种重要的化工产品,氨是氮肥工业及制造硝酸、铵盐、氮肥等重要原料,故B正确;
C.光照易爆炸,将氢气和氯气用点燃方法生成氯化氢,溶于水制得盐酸,故C错误;
D.制造普通水泥的主要原料是粘土、石灰石,在水泥回转窑中反应生成水泥,故D正确;
故选C.
点评 本题考查玻璃、氨的用途、盐酸的制备、水泥的原料等知识,题目难度不大,注意掌握常见物质的工业制备的原理.

练习册系列答案
相关题目
15.一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体质量为67.2g,当其缓慢经过无水CaCl2时,CaCl2增重32.4g,则原混合气体中CO2的质量为( )
| A. | 8.4 g | B. | 26.4 g | C. | 30.2 g | D. | 34.8 g |
16.下列各装置能构成原电池的是( )
| A. | 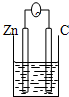 稀硫酸 | B. | 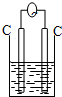 AgNO3(aq) | C. | 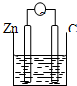 蔗糖 | D. | 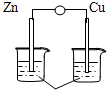 稀硫酸 |
13.根据下列实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将某溶液与稀盐酸反应产生的气体通入澄清石灰水 | 石灰水变浑浊 | 该溶液中一定含有CO32- |
| B | 常温下,将铁片浸入足量浓硫酸中 | 铁片不溶解 | 常温下,铁与浓硫酸一定没有发生化学反应 |
| C | 向某食盐溶液中滴加淀粉溶液 | 溶液颜色不变 | 该实验中一定没有添加KIO3 |
| D | 向苯酚钠溶液滴加乙酸溶液 | 溶液变浑浊 | 相同条件下,乙酸的酸性一定比苯酚强 |
| A. | A | B. | B | C. | C | D. | D |
20.下列物质中,只含有共价键,不含有离子键的是( )
| A. | Na2O2 | B. | KOH | C. | CaCl2 | D. | CO2 |
10.下列各组三种元素中,属于同一周期的是( )
| A. | C、H、O | B. | F、Cl、Br | C. | Li、Be、B | D. | Si、S、P |
17.下列叙述正确的是( )
| A. | 离子键只有饱和性没有方向性 | B. | 离子晶体中只含有离子键 | ||
| C. | 离子键的强弱可用晶格能来衡量 | D. | 离子键的强弱可用原子化热来衡量 |
14.有关能量的判断或表示方法正确的是( )
| A. | 由H+(aq)+OH-(aq)═H2O△H=-57.3 kJ/mol可知:含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出热量等于57.3 kJ | |
| B. | 从C(石墨)═C(金刚石)△H=+1.19 kJ/mol可知:金刚石比石墨更稳定 | |
| C. | 等质量的硫蒸气和硫固体分别完全燃烧,前者放出热量更多 | |
| D. | 2 g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol-1 |
15.下列有关说法正确的是( )
| A. | 饱和氯水中Cl-、NO3-、Na+、SO32-可以大量存在 | |
| B. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| C. | 向无色溶液中滴加氯水和CCl4,振荡,静置,下层溶液显紫色,说明原溶液中有I- | |
| D. | SO2通入碘水中,反应的离子方程式为SO2+I2+2H2O=SO32-+2I-+4H+ |