题目内容
10.以下电子排布式是激发态原子的电子排布的是( )| A. | 1s22s1 | B. | 1s22s22p1 | C. | 1s22s22p63s2 | D. | 1s22s22p63p1 |
分析 原子的核外电子排布符合基态原子核外电子填充的能级顺序和能量最低原理、泡利不相容原理及洪特规则,原子处于基态,否则为激发态,以此进行判断.
解答 解:基态原子的电子排布式符合能量最低原理,A、B、C项均为基态;D项1s22s22p63p1为激发态,根据能量最低原理,其基态应为1s22s22p63s1.
故选D.
点评 本题考查原子核外电子的排布,侧重于激发态的判断,可根据能量最低原理进行判断,题目难度不大.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
1.下列叙述中,正确的是( )
①AlCl3溶液蒸干灼烧得到氧化铝 ②碳酸钠溶液中离子共有4种
③电镀时应把镀件置于电解槽的阴极 ④冶炼铝时,把氧化铝加热成为熔融体后电解
⑤钢铁表面常易腐蚀生成Fe2O3•nH2O ⑥催化剂降低了活化能,故可以改变化学反应限度.
①AlCl3溶液蒸干灼烧得到氧化铝 ②碳酸钠溶液中离子共有4种
③电镀时应把镀件置于电解槽的阴极 ④冶炼铝时,把氧化铝加热成为熔融体后电解
⑤钢铁表面常易腐蚀生成Fe2O3•nH2O ⑥催化剂降低了活化能,故可以改变化学反应限度.
| A. | ①③④⑤ | B. | ①②③④⑤ | C. | ①③⑤⑥ | D. | ②④ |
18.R、W、X、Y、Z为原子序数依次递增的同一周期元素,下列说法一定正确的是(m、n均为正整数 )( )
| A. | 若Y的最低化合价为-2,则Z的最高正化合价为+6 | |
| B. | 若X的最高正化合价为+5,则五种元素都是非金属元素 | |
| C. | 若R(OH)n 为强碱,则W(OH)n+1也为强碱 | |
| D. | 若HnXOm为强酸,则Y是活泼非金属元素 |
15.已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是( )
| A. | KClO3是氧化剂 | |
| B. | 被氧化与被还原的氯元素的质量比为5:1 | |
| C. | H2SO4既不是氧化剂又不是还原剂 | |
| D. | 0.5mol KClO3参加反应时有5mol电子转移 |
19.交警检查司机是否酒后驾车的方法是让司机呼出的气体接触强氧化剂重铬酸钾,通过重铬酸钾颜色的变化来判断是否酒后驾车.如果司机是酒后驾车则酒精在仪器中发生了( )
| A. | 氧化反应 | B. | 还原反应 | C. | 消去反应 | D. | 酯化反应 |
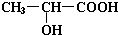 .
.