题目内容
20.由葡萄糖发酵可得乳酸,为研究乳酸的分子组成和结构,进行了下述实验:(1)称取乳酸0.9g,在某种状况下使其完全气化,相同状况下同体积的H2的质量为0.02g,则乳酸的相对分子质量为90.
(2)若将上述乳酸蒸气在氧气中燃烧只生成CO2和H2O(g),当全部被碱石灰吸收时,碱石灰的质量增加1.86g;若将此产物通入过量石灰水中,则产生3.00g白色沉淀.则乳酸的分子式为C3H6O3.
(3)另取0.90g乳酸,若与足量金属钠反应,生成H2 224mL(标准状况),若与足量碳酸钠反应,生成112mL CO2(标准状况),则乳酸的结构简式可能为CH2(OH)CH2COOH或
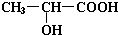 .
.(4)若葡萄糖发酵只生成乳酸,其反应的化学方程式为C6H12O6 (葡萄糖)$\stackrel{乳酸菌}{→}$2CH3CH(OH)COOH或C6H12O6 (葡萄糖)$\stackrel{乳酸菌}{→}$2HOCH2CH2COOH.
分析 (1)相对分子质量之比等于其密度之比;
(2)3.00g白色沉淀为碳酸钙,碱石灰增重为乳酸生成二氧化碳与水的总质量,计算二氧化碳、乳酸的物质的量,进而计算燃烧生成水的质量,根据原子守恒计算分子中C、H原子数目,再根据相对分子质量计算O原子数目,进而确定分子式;
(3)乳酸为0.01mol,与碳酸钠反应生成二氧化碳为0.005mol二氧化碳,说明乳酸分子含有1个-COOH,与钠反应生成0.01mol氢气,则说明还含有一个-OH,结合分子式书写可能的结构简式;
(4)结合(3)中乳酸的可能结构书写方程式.
解答 解:(1)相对分子质量之比等于密度之比,则Mr(乳酸):2=0.9g:0.02g,故Mr(乳酸)=90,故答案为:90;
(2)3.00g白色沉淀为碳酸钙,物质的量为$\frac{3g}{100g/mol}$=0.03mol,乳酸的物质的量为$\frac{0.9g}{90g/mol}$=0.01mol,0.01mol乳酸完全燃烧生成CO2 0.03 mol,则乳酸分子中C原子数目为$\frac{0.03mol}{0.01mol}$=3,生成H2O的质量=1.86g-0.03mol×44g/mol=0.54g,其物质的量为$\frac{0.54g}{18g/mol}$=0.03 mol,乳酸分子中H原子数目为$\frac{0.03mol×2}{0.01mol}$=6,则乳酸分子中O原子数目为$\frac{90-12×3-6}{16}$=3,所以乳酸的分子式为C3H6O3,
故答案为:C3H6O3;
(3)乳酸的物质的量为$\frac{0.9g}{90g/mol}$=0.01mol,与碳酸钠反应生成二氧化碳为$\frac{0.112L}{22.4L/mol}$=0.005mol,由于2-COOH~CO2↑,则乳酸分子含有1个-COOH,与钠反应生成氢气为$\frac{0.224L}{22.4L/mol}$=0.01mol,2-COOH~H2↑,2-OH~H2↑,可知乳酸分子还含有一个-OH,可知乳酸的结构简式可能是CH2(OH)CH2COOH或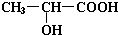 ,
,
故答案为:CH2(OH)CH2COOH;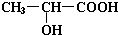 ;
;
(4)若葡萄糖发酵只生成乳酸,其反应的化学方程式为:C6H12O6 (葡萄糖)$\stackrel{乳酸菌}{→}$2CH3CH(OH)COOH或C6H12O6 (葡萄糖)$\stackrel{乳酸菌}{→}$2HOCH2CH2COOH,
故答案为:C6H12O6 (葡萄糖)$\stackrel{乳酸菌}{→}$2CH3CH(OH)COOH或C6H12O6 (葡萄糖)$\stackrel{乳酸菌}{→}$2HOCH2CH2COOH.
点评 本题考查有机物分子式确定、结构式的确定,属于计算推断,题目难度中等,注意掌握官能团的性质.

 阅读快车系列答案
阅读快车系列答案| A. | 1s22s1 | B. | 1s22s22p1 | C. | 1s22s22p63s2 | D. | 1s22s22p63p1 |
Ce 4++Fe 2+═Fe 3++Ce 3+
Sn 2++2Fe 3+═2Fe 2++Sn 4+
由此可以确定Fe 2+、Ce 3+、Sn 2+三种离子的还原性由强到弱的顺序是( )
| A. | Sn 2+、Fe 2+、Ce 3+ | B. | Sn 2+、Ce 3+、Fe 2+ | ||
| C. | Ce 3+、Fe 2+、Sn 2+ | D. | Fe 2+、Sn 2+、Ce 3+ |
| A. | $\stackrel{+4}{Mn}$O2→$\stackrel{+2}{Mn}$SO4 | B. | Al 2O 3→Al(OH) 3 | C. | $\stackrel{-1}{KI}$→K$\stackrel{+5}{I}$O3 | D. | HNO 3→NO |
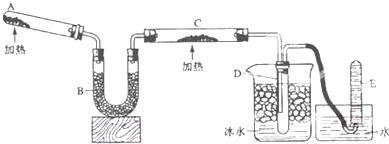
 如图所示装置,回答下列问题:
如图所示装置,回答下列问题: 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白: 如图是三种类别的烃CnH m分子中碳原子数n(C原子)与含碳量C%的关系.
如图是三种类别的烃CnH m分子中碳原子数n(C原子)与含碳量C%的关系.