题目内容
过氧化钙(CaO2)是一种安全无毒物质,带有数量不等的结晶水,通常还含部分CaO。已知:2CaO2·nH2O 2CaO+O2↑+2nH2O,2CaO2+4HCl=2CaCl2+2H2O+O2↑。现称取2.168 g过氧化钙样品分成两等份进行下列实验:
2CaO+O2↑+2nH2O,2CaO2+4HCl=2CaCl2+2H2O+O2↑。现称取2.168 g过氧化钙样品分成两等份进行下列实验:
实验一:将一份过氧化钙样品充分灼热,结果得到的O2在标准状况下体积为134.4 mL。
实验二:将另一份样品溶于适量的稀盐酸中,充分反应后,加入足量的Na2CO3溶液,结果得到1.40 g沉淀。
(1)试计算2.168 g样品中CaO的质量.
(2)试计算样品中CaO2·nH2O的n值。
(1)一份中:n(CaO2·nH2O)=2n(O2)=0.012mol(1分)n(CaCO3)=0.014mol(1分)
n(CaO)=n(CaCO3)- n(CaO2·nH2O)=0.002mol(1分)2.168 g
样品中m(CaO)=0.002mol×56g/ mol×2="0.224" g(2分)
(2)2×0.012×(72+18n)=2.168- 0.224 n=0.5(3分)
解析试题分析:(1)n(O2)=0.1344L/22.4L/mol=0.006mol
一份中:n(CaO2?nH2O)=2n(O2)=0.012mol,n(CaCO3)=0.014mol ,
n(CaO)=n(CaCO3)-n(CaO2?nH2O)=0.002mol,2.168 g样品中m(CaO)=0.002mol×56g/mol×2=0.224g,答:2.168g样品中CaO的质量为0.224g,(2)2.168g过氧化钙样品中的质量为2.168g-0.224g,则2×0.012×(72+18n)=2.168-0.224,n=0.5,答:样品中CaO2?nH2O的n值为0.5.
考点:本题考查化学方程式的计算,题目难度不大,注意根据物质的质量关系结合质量守恒根据方程式计算.

在给定温度和压强下的理想气体,影响其所占体积大小的主要因素是:
| A.分子直径的大小 | B.分子间的距离 |
| C.分子数目的多少 | D.分子间引力的大小 |
现有CuO、FeO、Fe2O3组成的混合物m g,向其中加入100mL 3mol·L-1硫酸,恰好完全溶解,若mg该混合物在过量氢气流中加热充分反应,则冷却后剩余固体的质量为
| A.(m-1.6)g | B.(m-2.4)g | C.(m-4.8)g | D.无法计算 |
下列有关化学用语表示正确的是( )
A.四氯化碳分子比例模型: |
| B.次氯酸的结构式为 H-Cl-O |
C.COS的电子式是 |
D.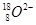 离子结构示意图: 离子结构示意图: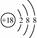 |
设NA为阿伏加德罗常数的值,下列叙述不正确的
| A.5g质量分数为46%的乙醇溶液中,氢原子的总数为0.6NA |
| B.5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA |
| C.50 mL 12 mol?L-1浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| D.常温常压下,46g NO2 与N2O4的混合气体中含有的原子总数为3NA |
HF气体分子间容易缔合。某HF气体由HF、(HF)2、 (HF)3三者混合而成,其平均相对分子质量为42,则(HF)3的体积分数可能为
| A.51% | B.56% | C.49% | D.10% |
设NA表示阿伏加德罗常数的值。下列说法正确的是
| A.5.6 g Fe与足量稀HNO3发生反应,转移的电子数为0.3 NA |
| B.在1 L 0.1 mol/L AlCl3溶液中含有0.1 NA个Al3+ |
| C.在某密闭容器中盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应后,可得0.2 NA个NH3分子 |
| D.标准状况下,11.2 L四氯化碳中含有的C—Cl键的个数为2 NA |
下列有关化学用语表示正确的是
A.氢氧化钠的电子式: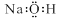 |
B.Cl-的结构示意图: |
C.2-丁醇的结构简式: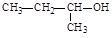 |
| D.碳酸的电离方程式:H2CO3=2H++CO32- |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果不正确的是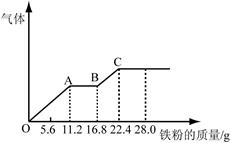
| A.混合酸中HNO3物质的量浓度为2 mol·L-1 |
| B.原混合酸中H2SO4物质的量为0.4 mol |
| C.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| D.第二份溶液中最终溶质为FeSO4 |