题目内容
设NA为阿伏加德罗常数的值,下列叙述不正确的
| A.5g质量分数为46%的乙醇溶液中,氢原子的总数为0.6NA |
| B.5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA |
| C.50 mL 12 mol?L-1浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| D.常温常压下,46g NO2 与N2O4的混合气体中含有的原子总数为3NA |
C
解析试题分析:A、5g质量分数为46%的乙醇溶液中,乙醇的质量=5g×46%=2.3g,物质的量=2.3g÷46g/mol=0.05mol,氢原子的物质的量=0.05mol×6=0.3mol。水的质量=5g-2.3g=2.7g,水的物质的量=2.7g÷18g/mol=0.15mol,氢原子的物质的量=0.15mol×2=0.3mol,所以氢原子总的物质的量是0.6mol,则氢原子的总数为0.6NA,A正确;B、5.6g铁的物质的量是0.1mol,与0.1mol氯气反应时铁过量,氯气完全反应,所以反应中转移电子数为0.2NA,C不正确;D、NO2与N2O4的最简式相同,均是NO2,所以46g NO2 与N2O4的混合气体中含有的原子的物质的量=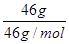 ×3=3mol,其原子总数为3NA,D正确,答案选C。
×3=3mol,其原子总数为3NA,D正确,答案选C。
考点:考查阿伏加德罗常数的有关计算

练习册系列答案
相关题目
某结晶水合物的化学式为R·nH2O,其相对分子质量为M。25 ℃时,a g该晶体能够溶于b g水中形成V mL溶液。下列关系中不正确的是
A.该溶液中溶质的质量分数为 |
B.该溶液的物质的量浓度为 |
C.该溶液中溶质与溶剂的质量比为 |
D.该溶液的密度为 |
同温同压下,等质量的SO2气体和SO3气体相比较,下列叙述中正确的是( )
| A.密度比为4:5 | B.物质的量之比为4:5 |
| C.体积比为1:1 | D.原子数之比为3:4 |
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图。反应中镁和铝的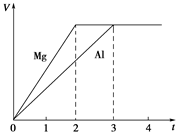
| A.物质的量之比为3∶2 |
| B.质量之比为3∶2 |
| C.摩尔质量之比为2∶3 |
| D.反应速率之比为2∶3 |
用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A.标准状况下,22.4L乙醇完全燃烧后生成CO2的分子数为2NA |
| B.56g的铁发生氧化还原反应,一定失去3NA个电子 |
| C.标准状况下,22.4L氟气中所含氟原子数为2NA |
D.0.1mol·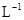 稀硫酸中含有 稀硫酸中含有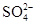 离子数为0.1NA 离子数为0.1NA |
往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示。则原溶液中c(I-)/c(Cl-)的比值为( ) 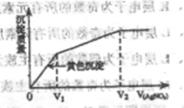
| A.(V2-V1)V1 | B.V1/V2 |
| C.V1/(V2-V1) | D.V2/V1 |
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
| A.16. 9 g过氯化钡(BaO2)固体中阴、阳离子总数约为0. 2NA |
| B.常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA |
| C.a g某气体含分子数为b,c g该气体在标况下的体积为22. 4bc/ aNAL |
| D.某密闭容器盛有0. l molN2和0. 3 mol H2,在一定条件下充分反应,转移电子的数目为0. 6NA |
 2CaO+O2↑+2nH2O,2CaO2+4HCl=2CaCl2+2H2O+O2↑。现称取2.168 g过氧化钙样品分成两等份进行下列实验:
2CaO+O2↑+2nH2O,2CaO2+4HCl=2CaCl2+2H2O+O2↑。现称取2.168 g过氧化钙样品分成两等份进行下列实验: ;
; ;
;