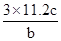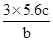题目内容
足量的铜与一定量的浓硝酸反应得到硝酸铜溶液和NO、N2O4、NO2的混合气体,这些气体与1.68升O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。则和铜反应的硝酸的物质的量可能是( )
| A.0.4mol | B.0.55mol | C.0.6mol | D.0.65mol |
B
解析试题分析:由题知,铜化合价升高数=硝酸化合价降低数=氧气化合价降低数=1.68*4/22.4=0.3(mol).
n铜=0.3/2=0.15(mol).和铜反应的硝酸的物质的量=生成Cu(NO3 ) 2的硝酸的物质的量+发生还原反应的硝酸的物质的量
(1) 硝酸被还原为NO,硝酸的物质的量为:0.15*2+0.3/3=0.4(mol).
(2) 硝酸被还原为N2O4、NO2,硝酸的物质的量为:0.15*2+0.3=0.6(mol).
(3) 硝酸被还原为NO、N2O4、NO2的混合气体,硝酸的物质的量为:在0.4-0.6之间。选B
考点:考查关于氧化还原反应化合价升降数等的化学计算等相关知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,5.6L CH4含C—H键数目为NA |
| B.常温常压下,100g17%H2O2水溶液含氧原子总数为NA |
| C.标准状况下,5.6L O2与适量Na加热反应,转移电子数一定为NA |
| D.常温常压下,14g乙烯与丙烯的混合气体,含碳原子总数为NA |
11.9g金属锡(Sn)跟100mL12mol·L-1HNO3共热一段时间。完全反应后测定溶液中c(H+)为8mol·L-1,溶液体积仍为100mL。产生的气体全部被氢氧化钠溶液吸收,消耗氢氧化钠0.4mol。由此推断氧化产物可能是
| A.SnO2·4H2O | B.Sn(NO3)4 |
| C.Sn(NO3)2 | D.Sn(NO3)2和Sn(NO3)4 |
下列有关化学用语表示正确的是
A.四氯化碳分子比例模型: |
| B.次氯酸的结构式为 H-Cl-O |
C.COS的电子式是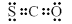 |
D.O2-离子结构示意图: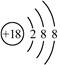 |
下列关系正确的是
| A.等物质的量的Na2O2与Na2O 中阴离子个数之比为2:1 |
| B.标准状况下,等体积的CO2与CO中氧原子数之比为2:1 |
| C.pH相同的H2SO4(aq)与CH3COOH(aq)中的c(H+)之比为2:1 |
| D.等浓度的(NH4)2SO4 (aq)与NH4Cl(aq)中c(NH4+)之比为2:1 |
设NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.1 mol NaHCO3固体中含有NA个CO32- |
| B.1 mol CH3C1中所含的共价键数为4NA |
| C.常温下,稀释一定浓度的CH3COOH溶液,溶液的pH增大,CH3COOH的电离常数减小 |
| D.欲配制0.1mol ?L-1的CuSO4溶液,只需将25. 0 gCuSO4·5H2O溶于1 L水中即可 |
下列化学用语正确的是 ( )
| A.HCN分子的结构式:H-C≡N |
| B.乙烯的结构简式:CH2CH2 |
C.F-离子结构示意图: |
D.二氧化碳的电子式: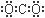 |
将amol小苏打和bmol过氧化钠置于某体积可变的密闭容器中充分加热,反应后测得容器内的氧气为1 mol,下列说法一定正确的是
| A.b="2" |
| B.反应中转移的电子数一定为2NA |
| C.容器中一定没有残余的CO2和水蒸气 |
| D.a:b≥1 |