题目内容
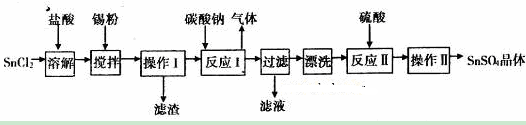
硫酸铜是一种应用广泛的化工原料,实验室中可通过不同途径制取硫酸铜溶液和胆矾(CuSO4·5H2O),其中一种流程如下:
(1)操作Ⅰ具体为 、 、过滤、烘干。
(2)杂铜(含少量有机物)灼烧后的产物除氧化铜还含少量铜,原因可能是 (填字母代号)。
| A.灼烧过程中部分氧化铜被还原 |
| B.灼烧不充分,铜未被完全氧化 |
| C.氧化铜在加热过程中分解生成铜 |
| D.该条件下铜无法被氧气氧化 |
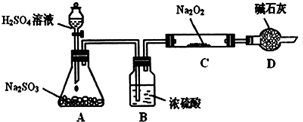
(4)通过下述图1装置也可制取硫酸铜溶液(已知:2NaOH+2NO2
 NaNO3+NaNO2+H2O)。
NaNO3+NaNO2+H2O)。

图1 图2
烧瓶内发生反应的离子方程式为 ;
图2是图1的改进装置,其优点有:① ;② 。
(1)蒸发浓缩 冷却结晶
(2)AB
(3)CuO(其他合理答案也可) Fe(OH)3
(4)Cu+4H++2N
 Cu2++2NO2↑+2H2O
Cu2++2NO2↑+2H2O
3Cu+8H++2N
 3Cu2++2NO↑+4H2O(写出一个即可) ①防止氢氧化钠溶液倒吸进入发生装置 ②NO、NO2气体被完全吸收
3Cu2++2NO↑+4H2O(写出一个即可) ①防止氢氧化钠溶液倒吸进入发生装置 ②NO、NO2气体被完全吸收
解析

苯甲酸是一种重要的化工产品,某学习小组设计方案制备苯甲酸。反应原理如下: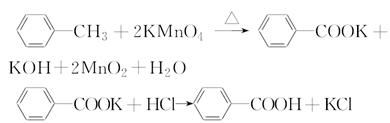
已知甲苯的熔点为-95℃,沸点为110.6℃,易挥发,密度为0.866 g·cm-3;苯甲酸的熔点为122.4℃,在25℃和95℃下溶解度分别为0.3 g和6.9 g。
【制备产品】 30.0 mL甲苯和25.0 mL 1 mol·L-1高锰酸钾溶液在80℃下反应30 min,装置如图所示:
(1)图中支管的作用是_______________________。
(2)冷凝管的作用是________;进水口为________(填“a”或“b”)。
(3)相对于用酒精灯直接加热,用沸水浴加热的优点是________;在本实验中,三颈烧瓶最合适的容积是________(填字母)。
| A.50 mL | B.100 mL | C.200 mL | D.250 mL |
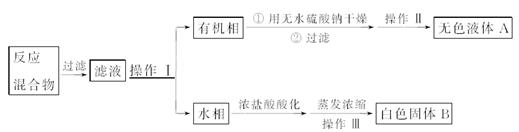
(4)操作Ⅰ的名称是________;含有杂质的产物经操作Ⅱ进一步提纯得无色液体A,则操作Ⅱ的名称是________。
(5)操作Ⅲ的名称是________。检验B中是否含有Cl-的方法如下:取少量B溶于水,在上层清液中滴加稀硝酸酸化的________溶液,若产生白色沉淀,则B中含有Cl-。
某种粗盐中含有泥沙、Ca2+、Mg2+、Fe3+、SO等杂质。某同学在实验室中设计了用这种粗盐制备精盐的方案如下(用于沉淀的试剂稍过量):
请回答以下问题:
(1)为操作Ⅳ选择所需仪器(用标号字母填写):________。
| A.烧杯 | B.试管 | C.玻璃棒 | D.分液漏斗 E.漏斗 F.酒精灯 |
(2)操作Ⅲ中常用Na2CO3溶液、NaOH溶液、BaCl2溶液作为除杂试剂,则加入除杂试剂的顺序为:NaOH溶液→________→________。
(3)操作Ⅲ中,判断加入BaCl2已过量的方法是_________________________。
(4)操作Ⅴ应选择的酸是________,若将操作Ⅴ与操作Ⅳ的先后顺序对调,将会对实验结果产生的影响是__________________________________________。
(5)操作Ⅵ是________(选择合理操作的名称,用标号字母按操作先后顺序填写)。
a.过滤、洗涤 b.蒸发、浓缩 c.萃取、分液 d.冷却、结晶
草酸(H2C2O4)是一种弱酸,在工业中有重要作用。某同学查资料得知“菠菜中富含可溶性草酸盐和碳酸盐”,他将菠菜研磨成汁,热水浸泡,经过滤得到溶液,加入足量的CaCl2溶液,产生白色沉淀,过滤、洗涤沉淀备用,然后对生成的沉淀进行探究。
(1)草酸盐溶液呈弱碱性的原因是_____________________________________。
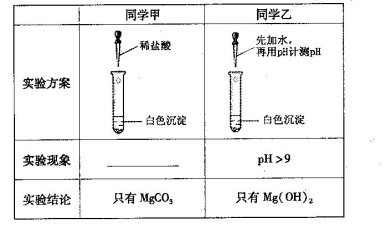
(2)该同学对生成的沉淀进行定性探究。
①提出合理假设。
假设1:只存在CaCO3;
假设2:既存在CaCO3,也存在CaC2O4;
假设3:___________________________________________________________。
②基于假设2,设计实验方案,进行实验。请在下表中写出实验步骤以及预期现象和结论。限选实验试剂:
1 mol·L-1 H2SO4、0.1 mol·L-1盐酸、0.01 mol·L-1 KMnO4溶液、澄清石灰水。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量沉淀于试管中,加入_________________________________ ________________________________ | _______________________________ _______________________________ 说明沉淀中有CaCO3 |
| 步骤2:_________________________ ________________________________ | ________________________________ |
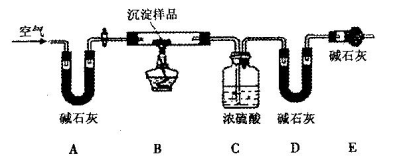
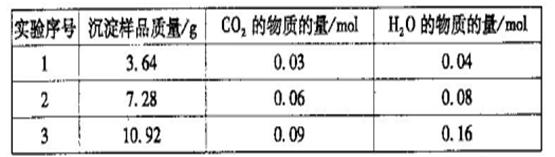
(3)基于假设3,另一位同学对生成的沉淀进行定量探究。用稀盐酸溶解生成的沉淀,并加水配制成100 mL溶液。每次准确移取25.00 mL该溶液,用0.010 mol·L-1 KMnO4标准溶液滴定,平均消耗标准溶液V mL。若菠菜样品的质量为m g,则菠菜中草酸及草酸盐(以C2O42—计)的质量分数为________。
某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量都在10%以上.某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在.
所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3·H2O.
该小组探究过程如下:
●查阅资料:
| ①镁、铝、锌都是银白色的金属; ②锌(Zn)可以与NaOH溶液反应生成H2; ③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3·H2O; ④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH4+. |
(1)假设①:该混合金属粉末中除镁外还含有________元素
假设②:该混合金属粉末中除镁外还含有________元素
假设③:该混合金属粉末中除镁外还含有铝、锌元素
●实验探究:
甲同学基于假设③设计实验方案如下:
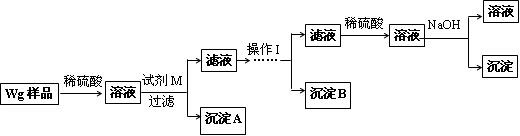
乙同学同样基于假设3设计另一实验方案如下:
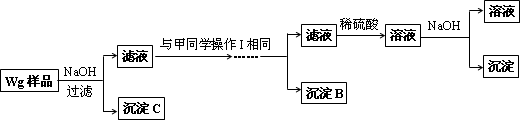
(2)试剂M是____________,沉淀B是_____________.
(2)试剂M是____________,沉淀B是_____________.
(3)丙同学认为乙同学的方案比甲同学的好,理由是_______________________.
(4)丁同学研究了甲、乙两同学的方案后,在其中一种方案的基础上用最简便方法测定了Wg样品中金属镁(Mg)的质量,他的方法是____________________________.
(5)操作Ⅰ的主要过程是:在滤液中逐滴加入_______________,直至生成的沉淀刚好溶解,再加入足量的____________________.