题目内容
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A.常温常压下,11.2L氧气所含的原子数为NA
B.1.7g的NH+4离子中含有的电子数为NA
C.常温常压下,48gO3含有的氧原子数为3NA
D.2.4g金属镁变为镁离子时失去的电子数为0.1NA
【答案】C
【解析】
A.不是标准状况,不能使用气体摩尔体积Vm=22.4L/mol,11.2L氧气的物质的量不是0.5mol,所含的原子数不是NA,故A错误;
B.1.8g的NH4+含有的NH4+数目为N(NH4+)=![]() =0.1NA,电子的数目为10×0.1NA=NA,故B错误;
=0.1NA,电子的数目为10×0.1NA=NA,故B错误;
C.n(O)=![]() =3mol,48gO3含有的氧原子数为N(O)=n(O)NA=3mol×NAmol1=3NA,故C正确;
=3mol,48gO3含有的氧原子数为N(O)=n(O)NA=3mol×NAmol1=3NA,故C正确;
D.2.4g金属镁含有镁原子数目N(Mg)=![]() =0.1NA,失去电子数为2×0.1NA=0.2NA,故D错误;
=0.1NA,失去电子数为2×0.1NA=0.2NA,故D错误;
答案选C。

练习册系列答案
相关题目
【题目】如图图象中,纵坐标为沉淀物的物质的量,横坐标为向溶液中加入反应物的物质的量,则相应的图像序号与(1)—(4)对应的是
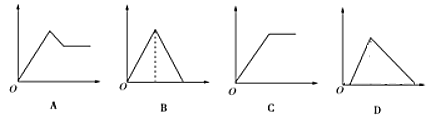
溶液 | 加入物质 | 对应的图像 |
(1)饱和石灰水 | 通过量CO2气体 | ____ |
(2)氯化铝溶液 | 加入过量氨水 | ____ |
(3)MgCl2、AlCl3的混合液 | 逐滴加入NaOH溶液至过量 | ____ |
(4)含少量NaOH的NaAlO2溶液 | 逐滴加入稀盐酸 | ____ |