题目内容
14.已知NA代表阿伏加德罗常数,下列说法正确的是( )| A. | 在1L 0.1mol•L-1氟化钠溶液中含有F-和HF数目之和为0.1NA | |
| B. | 300mL 2mol/L蔗糖溶液中所含分子数为0.6NA | |
| C. | 标准状况下,1.8gD2O中含有NA个中子 | |
| D. | 标准状况下,2.24L三氯甲烷中含有氯原子数目为0.3NA |
分析 A、根据物料守恒来分析;
B、蔗糖溶液中,除了蔗糖分子外,还有水分子;
C、重水的摩尔质量为20g/mol;
D、标况下三氯甲烷为液态.
解答 解:A、在1L0.1mol/L的NaF溶液中,NaF的物质的量n=CV=0.1mol/L×1L=0.1mol,由于F-是弱酸根,在溶液中水水解为HF,根据F原子的守恒可知,F-和HF数目之和为0.1NA,故A正确;
B、蔗糖溶液中,除了蔗糖分子外,还有水分子,故溶液中的分子个数大于0.6NA个,故B错误;
C、重水的摩尔质量为20g/mol,故1.8g重水的物质的量为0.09mol,而1mol重水中含10mol中子,故0.09mol重水中含0.9NA个中子,故C错误;
D、标况下三氯甲烷为液态,故不能根据气体摩尔体积来计算其物质的量,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.0.9g某元素的单质直接跟氯气反应后,质量增加了3.55g,这种元素是( )
| A. | Na | B. | Mg | C. | Fe | D. | Al |
5.哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖.现向一密闭容器中充入1molN2和3molH2,在一定条下使该反应发生.下列有关说法正确的是( )
| A. | 达到化学平衡时,N2将完全转化为NH3 | |
| B. | 达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 | |
| C. | 达到化学平衡时,正反应和逆反应的速率都为零 | |
| D. | 达到化学平衡时,N2和H2的转化率相同且c(N2):c(H2)=1:3 |
2. 短周期元素X.Y.Z.W在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是( )
短周期元素X.Y.Z.W在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是( )
 短周期元素X.Y.Z.W在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是( )
短周期元素X.Y.Z.W在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是( )| A. | x与同主族且相邻元素的气态氢化物的沸点,前者高于后者 | |
| B. | 含Y元素的盐溶液有的显酸性,有的显碱性 | |
| C. | x的气态氢化物与w的最高价氧化物的水化物反应只能生成一种盐 | |
| D. | x与H、O元素形成的化合物可以组成一种盐,其中X.H.O元素原子个数之比为2:4:3 |
9.下列溶液中溶质的物质的量浓度为1mol•L-1的是( )
| A. | 将40gNaOH溶解于1L水中配成的NaOH溶液 | |
| B. | 常温常压下将22.4LHCl气体溶于水配成1L的盐酸溶液 | |
| C. | 将1 L0.5mol/L的浓盐酸加热浓缩为0.5L | |
| D. | 从1000mL 1mol/L NaCl溶液中取出100 mL的溶液 |
19.下列说法不正确的是( )
| A. | 钠和钾的合金可用于快中子反应堆作热交换剂 | |
| B. | 可用超纯硅制造的单晶硅来制芯片 | |
| C. | 可利用二氧化碳制造全降解塑料 | |
| D. | 氯气有毒,不能用于药物的合成 |
6.如表是元素周期表的一部分,表中所列的字母分别代表一种化学元素.试回答下列问题:
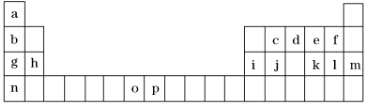
(1)元素p为26号元素,请写出其基态原子的电子排布式1s22s22p63s23p63d64s2.
(2)d与a反应的产物的分子中,中心原子的杂化形式为sp3.
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量.
(4)o、p两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难.对此,你的解释是Mn2+的3d轨道电子排布为半满状态,比较稳定.
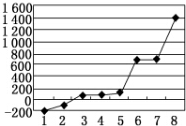
(5)第三周期8种元素按单质熔点高低的顺序如图所示,其中电负性最大的是2(填下图中的序号).
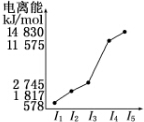
(6)表中所列的某主族元素的电离能情况如图所示,则该元素是Al(填元素符号).

(1)元素p为26号元素,请写出其基态原子的电子排布式1s22s22p63s23p63d64s2.
(2)d与a反应的产物的分子中,中心原子的杂化形式为sp3.
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量.
(4)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p | |
| 电离能kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
(5)第三周期8种元素按单质熔点高低的顺序如图所示,其中电负性最大的是2(填下图中的序号).

(6)表中所列的某主族元素的电离能情况如图所示,则该元素是Al(填元素符号).

3.下列有关高分子化合物的叙述正确的是( )
| A. | 高分子化合物极难溶解 | |
| B. | 高分子化合物依靠分子间作用力结合,材料强度较小 | |
| C. | 高分子均为长链状分子 | |
| D. | 高分子材料均为混合物 |
4.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温下,1L0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 1mol羟基中电子数为10 NA | |
| C. | 在反应KIO3+6HI═KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6 NA | |
| D. | 常温常压下,22.4L乙烯中C--H键数为4 NA |