题目内容
【题目】如图,锥形瓶内盛有气体X,滴管内盛有液体Y。若挤 压胶头滴管的胶头,使液体滴入瓶中,振荡,套在玻璃管一端的小气球慢慢鼓起,则气体X和液体Y不可能是

A. X是Cl2,Y是NaOH溶液
B. X是SO2,Y是澄清石灰水
C. X是NO,Y是水
D. X是NH3,Y是氯化钠溶液
【答案】C
【解析】
要使如图装置中的小气球鼓起来,则气体与滴加的液体反应或能溶于其中,使装置内气体体积减少,压强减小,据此进行分析解答。
A、氯气能与NaOH溶液反应,使装置内气体体积减少,压强减小,能使小气球a鼓起,故A不符合。
B、二氧化硫与石灰水反应,使装置内气体体积减少,压强减小,能使小气球a鼓起,故B不符合。
C、一氧化氮不能与水反应且不溶于水,装置内压强几乎无变化,不能使小气球a鼓起,故C符合。
D、氨气极易溶于氯化钠溶液,使装置内气体体积减少,压强减小,能使小气球a鼓起,故D不符合。
答案选C。

 阅读快车系列答案
阅读快车系列答案【题目】软锰矿的主要成分为MnO2,还含有MgO、CaO、FeO、Fe2O3、Al2O3等杂质,工业上用软锰矿制取MnSO4·H2O的流程如下:
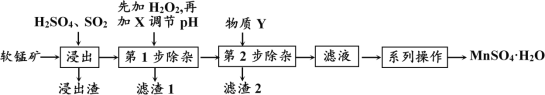
已知:① 几种常见金属离子形成氢氧化物沉淀时的pH值如下表:
氢氧化物 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Mg(OH)2 |
开始沉淀pH | 7.0 | 2.7 | 3.7 | 8.1 | 9.6 |
完全沉淀pH | 9.2 | 3.2 | 5.2 | 10.2 | 11 |
② 温度高于27℃时,MnSO4的溶解度随温度的升高而逐渐降低。
(1)已知:25℃、101kpa时,
Mn(s)+O2(g)=MnO2(s) △ H=-520 kJ/mol
S(s)+O2(g)=SO2(g) △ H=-297 kJ/mol
Mn(s)+S(s)+2O2(g)=MnSO4(aq) △ H=-1065 kJ/mol
“浸出”过程中MnO2转化为MnSO4的热化学方程式为___________________________。
(2) “第1步除杂”是为了除去浸出液中的Fe3+、Fe2+、Al3+,加入H2O2溶液的目的是(用离子方程式表示)____________________________________________,需要调节的pH的范围是_________________;所加的试剂X是_________ (填以下物质序号)。
A、MnO2 B、MnCO3 C、KMnO4 D、NaOH。
请用平衡移动原理分析,加入X能使除去浸出液中Fe3+的原因是:_______________。
(3)根据下表数据,选择“第2步除杂”所加的物质Y(由一种阳离子和一种阴离子组成),物质Y的化学式____________。
阴离子 Ksp 阳离子 | CO32- | F- | OH- |
Ca2+ | 5.0×10-9 | 1.5×10-10 | 4.7×10-6 |
Mg2+ | 3.8×10-6 | 7.4×10-11 | 5.6×10-12 |
Mn2+ | 2.2×10-11 | 5.3×10-3 | 2.1×10-13 |
(4)采用“系列操作”中需要“趁热过滤”,其目的是_______________________________。
(5)以MnSO4溶液为原料,采用电解的方法可制备高纯度的MnO2,则电解池阳极的电极反应方程式为___________________________________________________________。