题目内容
可以把6种无色溶液:乙醇、苯酚、NaHCO3溶液、AgNO3溶液、KOH溶液、氢硫酸一一区分的试剂是:
A.新制碱性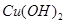 悬浊液 悬浊液 | B.FeCl3溶液 |
| C.BaCl2溶液 | D.酸性KMnO4溶液 |
B
试题分析:新制的氢氧化铜悬浊液只能和酸会含有醛基的有机物反应,因此不能鉴别这6种物质,所以A错误;苯酚和FeCl3溶液显紫色,乙醇和FeCl3溶液无明显现象,KOH溶液和FeCl3溶液有红褐色沉淀,AgNO3溶液和FeCl3溶液有白色沉淀,碳酸氢钠溶液和FeCl3溶液反应生成红褐色测定和CO2气体,和H2S反应生成单质S沉淀,现象各不相同,故B正确;氯化钡溶液只能和硝酸银溶液反应生成白色沉淀氯化银,因此不能鉴别这6种物质,所以C错误;乙醇、苯酚和H2S均能使酸性高锰酸钾溶液褪色。NaHCO3溶液、AgNO3溶液、KOH溶液与高锰酸钾不反应,不能鉴别这6这物质,所以D不正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题,侧重对学生分析、归纳和总结问题的能力的培养。答题时需要学生掌握好物质的性质与反应现象,要注意知识的总结和积累。该类试题需要注意的是进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目

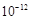
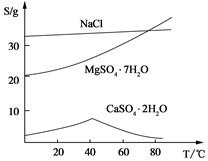
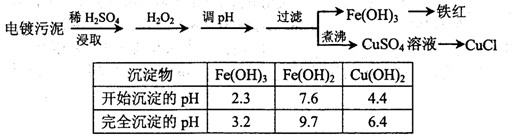
 Fe(OH)3+3H+,该反应的平衡常数为 。
Fe(OH)3+3H+,该反应的平衡常数为 。