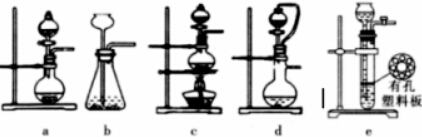
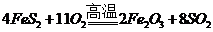��Ŀ����
14����ҵ���Դ�ͭΪԭ�ϲ�ȡ��ͼ��ʾ�����Ʊ�����ͭ���壺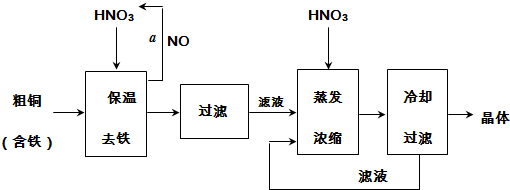
��1���ڲ���a�У�����Ҫͨ��������ˮ��������Ӧ�Ļ�ѧ����ʽ��4NO+3O2+2H2O=4HNO3��
��2���ڱ���ȥ���Ĺ����У�ΪʹFe3+������ȫ����������Һ�м���CuO��������Һ��pH�������±����ݣ���Һ��pHӦ������3.2��4.7��Χ����������Һ��pH=4����ʱ����Һ��c ��Fe3+��=4.0��10-6mol•L-1��[��֪�������£�Fe��OH��3��KSP=4.0��10-36]
| �������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
| Fe3+ Cu2+ | 1.9 4.7 | 3.2 6.7 |
��4����������Ũ��ʱ��Ҫ�������������Ա�����Һһ����c��H+������Ŀ���ǣ�������ӷ���ʽ��Ҫ˵��������Cu2+����ˮ�⣺Cu2++2H2O
 Cu��OH��2+2H+���������������������ͭ��ˮ�⣮
Cu��OH��2+2H+���������������������ͭ��ˮ�⣮��5����ҵ�ϳ���������ͭ��Һ���ͭ�����ʱ�����ĵ缫��Ӧʽ��Cu2++2e-=Cu��
���� ���Ʊ����̿�֪��Cu��Fe�������ᷴӦ��ΪʹFe3+������ȫ����������Һ�м���CuO��������Һ��pHΪ3.2��4.7������aΪ4NO+3O2+2H2O=4HNO3�����˳�ȥ������������Һ�к�����ͭ������������ͭ����ˮ�⣬����Ũ������ȴ�ᾧ�õ�����ͭ���壬�Դ������
��� �⣺���Ʊ����̿�֪��Cu��Fe�������ᷴӦ��ΪʹFe3+������ȫ����������Һ�м���CuO��������Һ��pHΪ3.2��4.7������aΪ4NO+3O2+2H2O=4HNO3�����˳�ȥ������������Һ�к�����ͭ������������ͭ����ˮ�⣬����Ũ������ȴ�ᾧ�õ�����ͭ���壬
��1��������������֪������a�У�����Ҫͨ��������ˮ��������Ӧ�Ļ�ѧ����ʽ��4NO+3O2+2H2O=4HNO3���ʴ�Ϊ��4NO+3O2+2H2O=4HNO3��
��2������Һ�м���CuO��������Һ��pHĿ����������ȫ��������ͭ���Ӳ�����������ͼ�����ݷ�����֪pHӦΪ3.2��4.7��������Һ��pH=4����ʱ����Һ��c ��Fe3+��=$\frac{4.0��1{0}^{-36}}{��1��1{0}^{-10}��^{3}}$=4.0��10-6mol•L-1���ʴ�Ϊ��3.2��4.7��4.0��10-6mol•L-1��
��3��Fe3+��ˮ�⣬Ϊ������Һ������Ũ����Ӧ������Ũ��Һ������ˮ�Ὣ��Һϡ�ͣ������ڽ���Һ����Ũ����
�ʴ�Ϊ����ˮ�Ὣ��Һϡ�ͣ������ڽ���Һ����Ũ����
��4����������Ũ��ʱ��Ҫ�������������Ա�����Һһ����c��H+������Ŀ��������Cu2+����ˮ�⣺Cu2++2H2O Cu��OH��2+2H+���������������������ͭ��ˮ�⣬�ʴ�Ϊ������Cu2+����ˮ�⣺Cu2++2H2O
Cu��OH��2+2H+���������������������ͭ��ˮ�⣬�ʴ�Ϊ������Cu2+����ˮ�⣺Cu2++2H2O Cu��OH��2+2H+���������������������ͭ��ˮ�⣻
Cu��OH��2+2H+���������������������ͭ��ˮ�⣻
��5������ͭ��Һ���ͭ�����ʱ�����ĵ缫��Ӧʽ��Cu2++2e-=Cu���ʴ�Ϊ��Cu2++2e-=Cu��
���� ���⿼�����ʵ��Ʊ�ʵ�鼰���������ᴿ���ۺ�Ӧ�ã�Ϊ��Ƶ���㣬�������ʵ����ʡ������еķ����ķ�Ӧ���������뷽��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��ˮ�⡢�绯ѧ��Ӧԭ����Ӧ�ã���Ŀ�ѶȲ���

 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�| A�� | Ħ���DZ�ʾ���������ĵ�λ | |
| B�� | 1mol���������2g | |
| C�� | O2��Ħ��������32g | |
| D�� | ÿĦ�����ʶ����а���٤��������ָ���� |
| A�� | 1 mol H2������ֻ���ڱ�״���²�ԼΪ2g | |
| B�� | �ڱ�״����ij����������22.4L������Ϊ����������ʵ���Լ��1mol | |
| C�� | ��20��ʱ��1mol�κ����������ܱ�22.4L�� | |
| D�� | 1mol H2��O2�Ļ���������������Ϊ34g |
| A�� | CH3COONa | B�� | NaHCO3 | C�� | NaCl | D�� | NH4Cl |
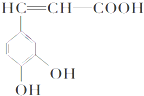 �����ᣨ��ͼ����������������ҩ����Ұ���ܲ�����Ҷˮ�ա�������У���������ֹѪ���ã����� ���ڿ������˵������ȷ���ǣ�������
�����ᣨ��ͼ����������������ҩ����Ұ���ܲ�����Ҷˮ�ա�������У���������ֹѪ���ã����� ���ڿ������˵������ȷ���ǣ�������| A�� | ������ķ���ʽΪC9H8O4 | |
| B�� | 1 mol��������Ժͺ�4 molBr2��Ũ��ˮ��Ӧ | |
| C�� | 1 mol������������NaHCO3��Һ��Ӧ�ܲ��������Լ67.2L��CO2 | |
| D�� | �������ø�����ؼ��鿧��������е�̼̼˫�� |
| A�� | �ж� | B�� | �ʻ���ɫ | ||
| C�� | ����ͬ��Ԫ�� | D�� | �ܺͽ������ʷ�Ӧ |
 A��B��C��D����Ԫ�صĺ˵������С��18��AԪ��ԭ�Ӻ���ֻ��1�����ӣ�B�ǵؿ��к�������Ԫ�أ�B��C���γ����ֻ�����CB��CB2��C���������������۾���ֵ��ȣ�CB�ж���CB2���������D+������Neԭ����ͬ�ĵ��Ӳ�ṹ��
A��B��C��D����Ԫ�صĺ˵������С��18��AԪ��ԭ�Ӻ���ֻ��1�����ӣ�B�ǵؿ��к�������Ԫ�أ�B��C���γ����ֻ�����CB��CB2��C���������������۾���ֵ��ȣ�CB�ж���CB2���������D+������Neԭ����ͬ�ĵ��Ӳ�ṹ��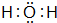 ��CB2�ĵ���ʽΪ
��CB2�ĵ���ʽΪ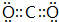 ��
��