题目内容
下列说法正确的是( )
| A.浓硫酸与亚硫酸钠反应制取二氧化硫,体现浓硫酸具有强氧化性 |
| B.铵盐受热易分解,均有NH3产生 |
| C.浓硝酸保存在棕色的细口瓶中 |
| D.化工厂可通过加高烟囱排放废气,防止形成酸雨 |
C
试题分析:A.Na2SO3 + H2SO4(浓)= Na2SO4+SO2↑+H2O.体现了浓硫酸具有强酸性。错误。B.铵盐受热易分解,但不是所有的铵盐分解都有NH3产生。错误。C.浓硝酸光照容易发生分解反应:4HNO3
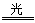 4NO2↑+2H2O。温度越高,浓度越大越容易分解。为了防止浓硝酸分解,所有应该保存在棕色的细口瓶中。正确。D.化工厂通过加高烟囱排放废气,只是减少在本地区的有害气体的含量,但是对于全局的环境保护无任何帮助。错误。
4NO2↑+2H2O。温度越高,浓度越大越容易分解。为了防止浓硝酸分解,所有应该保存在棕色的细口瓶中。正确。D.化工厂通过加高烟囱排放废气,只是减少在本地区的有害气体的含量,但是对于全局的环境保护无任何帮助。错误。
练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
 Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )
Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )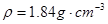 ) 60mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
) 60mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。