题目内容
【题目】硫酸锌是制造锌钡白和锌盐的主要原料,也可用于湿法电解制锌,如图为由锌灰制ZnSO4·7H2O晶体的工艺流程:
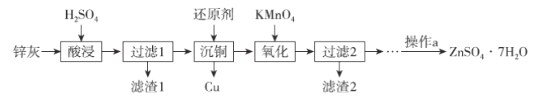
已知:①锌灰的主要成分为ZnO,还含有CuO、PbO、MnO和FeO;
②“滤渣2”的主要成分为Fe(OH)3和MnO(OH)2。
请回答下列问题:
(1)MnO(OH)2中Mn元素的化合价为_____________。
(2)“滤渣1”的主要成分为_____________。
(3)“氧化”时,需控制溶液的pH=5.1,Fe2+被氧化的离子方程式为_____________。
(4)操作a为_________、过滤、洗涤、干燥。
(5)ZnSO4·7H2O产品的纯度可用配位滴定法测定。准确称取一定量的ZnSO4·7H2O晶体加入250 mL的锥形瓶中,加水约20 mL,再加入2~3滴5%的二甲酚橙作指示剂、约5 mL六亚甲基四胺缓冲溶液,摇匀。用已标定的0.0160 mol/LEDTA溶液滴定,滴定至溶液由红紫色变成亮黄色,即为终点(ZnSO4·7H2O与EDTA按物质的量之比1:1反应)。实验数据如下表:
m(ZnSO4·7H2O)/g | 起始滴定管读数/mL | 终点滴定管读数/mL |
0.1692 | 0.20 | 26.50 |
ZnSO4·7H2O产品的纯度为_____________(保留2位有效数字)。
(6)工业上采用惰性电极作阳极电解ZnSO4溶液可实现湿法炼锌,电解过程中的离子方程式为___________。
【答案】+4 PbSO4 3Fe2++MnO4-+8H2O=3Fe(OH)3↓+MnO(OH)2↓+5H+ 蒸发浓缩、冷却结晶 71% 2Zn2++2H2O![]() 2Zn+4H+
2Zn+4H+
【解析】
钡白矿(锌灰的主要成分是ZnO,还含有CuO、PbO、MnO和FeO),加稀硫酸溶解,得到金属硫酸盐,PbSO4不溶,其余硫酸盐以溶于水,过滤,滤渣1为PbSO4,滤液中含有硫酸锌、CuSO4、FeSO4、MnSO4,加入锌粉发生置换反应:Zn+CuSO4=Cu+ZnSO4,滤渣为铜与过量的锌粉,滤液中再加高锰酸钾溶液,Fe2+与MnO4-反应生成Fe(OH)3、MnO(OH)2沉淀,滤渣2的主要成分为成Fe(OH)3、MnO(OH)2,过滤,滤液为硫酸锌,蒸发浓缩、冷却结晶、过滤得到ZnSO4·7H2O晶体。
(1)MnO(OH)2中Mn元素的化台价为+4价;
(2)根据上述分析可知“滤渣1”的主要成分为PbSO4;
(3)KMnO4具有强的氧化性,Fe2+具有还原性,在pH=5.1时,Fe2+被氧化产生Fe3+与溶液中OH-结合形成Fe(OH)3沉淀,MnO4-被还原产生MnO(OH)2 ,故根据电子守恒、电荷守恒、原子守恒,可得Fe2+被氧化的离子方程式为:3Fe2++MnO4-+8H2O=3Fe(OH)3↓+MnO(OH)2↓+5H+;
(4)滤液2主要成分是ZnSO4,由于ZnSO4的溶解度受温度的影响变化较大,所以从该溶液中得到硫酸锌晶体的操作a为蒸发浓缩、冷却结晶、过滤、洗涤、干燥;
(5)ZnSO4·7H2O与EDTA按物质的量之比1:1反应,根据表中数据,ZnSO4·7H2O产品的纯度为:![]() ×100%=71%;
×100%=71%;
(6)在工业上采用惰性电极作阳极电解ZnSO4溶液可实现湿法炼锌,阴极上Zn2+得到电子发生还原反应变为Zn单质,电极反应式为:Zn2++2e-=Zn,阳极上水电离产生的OH-失去电子发生氧化反应产生O2,电极反应式为:2H2O=O2↑+4H+,故电解过程中的离子方程式:2Zn2++2H2O![]() 2Zn+4H+。
2Zn+4H+。

【题目】类比推理是学习化学的重要的思维方法,下列陈述Ⅰ及类比推理陈述Ⅱ均正确的是( )
陈述Ⅰ | 类比推理陈述Ⅱ | |
A | 单质的熔点Br2 < I2 | 单质的熔点Li < Na |
B | 工业上电解熔融的Al2O3得到铝单质 | 工业上电解熔融的MgO得到镁单质 |
C | 还原性:I- > Br- | 还原性:P3- > N3- |
D | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
A.AB.BC.CD.D