题目内容
【题目】根据下列实验过程,请回答:
(1)在常温下,将氯气通入氢氧化钠溶液中,所发生反应的离子方程式为:__;所得溶液具有漂白性,其有效成分的名称为__。
(2)将上述呈碱性的溶液与FeCl3溶液混合,可制得一种新型绿色消毒剂——高铁酸钠(Na2FeO4),反应如下:3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O则该反应中的氧化产物是__(填离子符号),当反应中转移电子的数目是0.3NA时,所消耗的氧化剂的物质的量为__。
(3)证实最终所得溶液中含有Na+的操作是:进行焰色实验时,火焰呈现__色。
【答案】Cl2+2OH-=Cl-+ClO-+H2O 次氯酸钠 FeO42- 0.15mol 黄色
【解析】
(1)氯气通入氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;次氯酸钠具有氧化性,可作漂白剂;
(2)3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O反应中氯的化合价降低,得电子,被还原,铁元素的化合价升高被氧化,根据氧化还原反应化合价变化分析计算氧化剂的物质的量;
(3)钠元素在火焰上灼烧时的颜色为黄色。
(1)氯气通入氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,发生的离子反应为:Cl2+2OH-=Cl-+ClO-+H2O;次氯酸钠具有氧化性,可作漂白剂,所得溶液其有效成分的名称为次氯酸钠;
(2)3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O反应中氯的化合价降低,得电子,被还原,ClO-作氧化剂,对应产物Cl-为还原产物,铁元素的化合价升高被氧化,Fe3+作还原剂,对应产物FeO42-为氧化产物,根据反应氯元素有+1价变为-1价,3mol ClO-参与反应转移6mol电子,当反应中转移电子的数目是0.3NA,即0.3mol时消耗氧化剂的物质的量=![]() =0.15mol;
=0.15mol;
(3)钠元素在火焰上灼烧时的颜色为黄色,证实最终所得溶液中含有Na+的操作是:进行焰色实验时,火焰呈现黄色。

【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:取等物质的量浓度等体积H2O2溶液分别进行下列实验,实验报告如下表所示。

序号 | 条件 | 现象 | 结论 | |
温度/℃ | 催化剂 | |||
1 | 40 | FeCl3溶液 | ||
2 | 20 | FeCl3溶液 | ||
3 | 20 | MnO2 | ||
4 | 20 | 无 | ||
(1)实验1、2的目的是研究__________因素对H2O2分解速率的影响。
(2)实验1对应的化学方程式为___________________________。
实验二:经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图所示的实验。可通过观察_________得出结论。 有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是____________________。
实验三:已知在高锰酸钾(KMnO4)酸性溶液和草酸(H2C2O4)溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快。
(1)写出硫酸酸化的高锰酸钾溶液和草酸溶液反应的化学方程式____________
(2)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是______。
(3)若用实验证明你的猜想/span>,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是__________。
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰
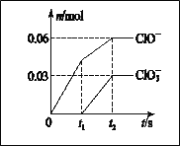
(4)若实验过程中将2.0mL0.10mol/LH2C2O4溶液与4.0mL0.010mol/L酸性KMnO4溶液混合(忽略溶液混合后体积的变化),测得溶液的褪色时间为40s,这段时间内平均反应速率v(KMnO4)=__________mol·L-1·min-1。