题目内容
几种短周期元素的原子半径及主要化合价见下表,根据表中信息,判断以下说法正确的是
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.111 | 0.104 | 0.143 | 0.066 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
B.离子半径: X2+>T2-
C.元素最高价氧化物对应的水化物的碱性:Y > R >X
D.相同条件下,等物质的量的单质与氢气化合放出能量的多少:T>Z
D
解析试题分析:由最高正价、原子半径推断,X、Y、Z、R、T分别是镁、铍、硫、铝、氧。镁的金属性比铝强,即金属性:X>R,故A错误;Mg2+、O2一都具有28电子层结构,但是前者的核电荷数大于后者,则镁离子半径小于氧离子半径,故B错误;镁的金属性比铝强,则氢氧化镁的碱性比氢氧化铝强,即X>R,故C错误;氧的非金属性比硫强,则等物质的量的氧气与氢气化合放出的能量多,故D正确。
考点:考查物质结构与元素周期律,涉及元素在周期表中位置、原子结构、元素及其化合物的主要性质之间的推断。

练习册系列答案
相关题目
下列说法错误的是
| A.H2O2和Na2O2都属于氧化物,两种物质中所含的化学键类型完全相同 |
| B.原子核外在离核较远区域的电子易失去,其原因是这些电子能量较高 |
| C.第三周期非金属元素形成氢化物的稳定性从左到右逐渐增强 |
| D.在周期表的金属元素和非金属元素的交界处寻找半导体,在过渡元素区中寻找催化剂 |
下列叙述与对应图式正确的是
A.由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强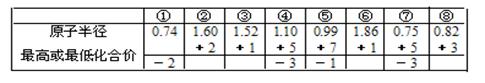 |
B.图甲表示Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2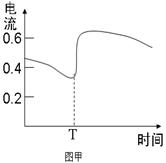  |
| C.图乙表示某一放热反应,若使用催化剂E1、E2、ΔH都会发生改变 |
| D.表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H= -571.6kJ/mol |
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是
| | Q | R | |
| T | | | W |
A.T的氧化物是光导纤维的主要成分
B.W的氢化物的化学式为HCl
C.R的最高正价氧化物的水化物是弱电解质
D.Q与氢形成的化合物均含极性共价键
下图为短周期的一部分,Y原子最外层电子数是其电子层数的2倍,下列说法正确的是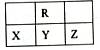
| A.Y的氢化物比Z的氢化物稳定 |
| B.原子半径大小顺序是X >Y>R |
| C.Y、R形成的化台物YR2能使酸性KMnO4溶液褪色 |
| D.四种元素中最高价氧化物的水化物的酸性最强的是Y |
下图为元素周期表中短周期的一部分,下列说法正确的是
| ① | ② | ③ |
| ④ | ⑤ | ⑥ |
A.①~⑥可能全部是非金属元素
B.对应单质的活泼性:②>③
C.④的最高价氧化物对应的水化物可能为两性物质
D.②、⑤的最高价氧化物对应的水化物可能均为强酸
X、Y、Z是位于同一周期的三种短周期元索,它们的最高价氧化物对应的水化物分别为:HXO4、H2YO4、H3ZO4,下列判断中错误的是
| A.原子半径:X>Y>Z | B.非金属性:X>Y>Z |
| C.气态氢化物稳定性:X>Y>Z | D.酸性:HXO4>H2YO4>H3ZO4 |
短周期元素M、W、X、Y、Z的原子序数依次增大,M元素的一种核素没有中子,且M、W、X、Y+、Z的最外层电子数与其电子层数的比值依次为1、2、3、4、2(不考虑零族元素)。下列关于这些元素的叙述正确的是
| A.X分别和其它四种元素均可形成至少2种化合物 |
| B.M分别和W、X、Y、Z形成化合物,均显相同化合价 |
| C.M、X、Z三种元素组成的化合物含有离子键 |
| D.M、X、Y组成化合物和Y、Z组成化合物,其水溶液均呈碱性 |
下列说法正确的是( )
| A.第ⅠA族金属单质的密度、熔沸点均随着核电荷数的增大而递增 |
| B.金属锂在氧气中燃烧生成Li2O2 |
| C.金属的还原性:Li>Na>K>Rb |
| D.氢化物的稳定性: HF > HCl > HBr > HI |