题目内容
【题目】已知某温度下,水的离子积常数KW=1.0×10-12,请回答下列问题:
(1)此温度___25℃(填“>”、“<”或“=”),原因是___。
(2)对水进行下列操作,能抑制水的电离的是___。
A.通入适量SO2气体 B.加入适量Ba(OH)2溶液
C.升温至60℃ D.加入NH4Cl溶液
(3)此温度下纯水中的c(H+)=__。
(4)醋酸的下列性质中,可以证明它是弱电解质的是___。
①1mol·L-1的CH3COOH溶液中c(H+)=10-2mol·L-1
②CH3COOH可以任意比与H2O互溶
③在相同条件下,CH3COOH溶液的导电性比盐酸弱
④10mL1mol/L的CH3COOH恰好与10mL1mol/L的NaOH溶液完全反应
⑤同浓度同体积的醋酸和盐酸与Fe反应时,醋酸溶液中放出H2的速度慢
⑥醋酸溶液中CH3COOH、CH3COO-、H+同时存在
【答案】> 水的离子积常数随温度的升高而增大 AB 1×10-6mol/L ①③⑤⑥
【解析】
已知某温度下,水的离子积常数KW=1.0×10-12,
⑴常温下水的离子积常数为KW=1.0×10-14,而此温度下,水的离子积常数KW=1.0×10-12,温度越高,离子积常数越大,从而说明此温度大于25℃,原因是水的离子积常数随温度的升高而增大,故答案为:>;水的离子积常数随温度的升高而增大;
⑵A选项,通入适量SO2气体,二氧化硫和水反应生成亚硫酸,电离出氢离子,抑制水的电离,故A符合题意;
B选项,加入适量Ba(OH)2溶液,电离出氢氧根离子,氢氧根离子浓度增大,平衡逆向移动,抑制水的电离,故B符合题意;
C选项,升温至60℃,平衡正向移动,促进水的电离,故C不符合题意;
D选项,加入NH4Cl溶液,铵根离子和水电离出的氢氧根离子结合生成弱电解质一水合氨,平衡正向移动,促进水的电离,故D不符合题意;
综上所述,答案为:AB;
⑶水的离子积常数KW=1.0×10-12,此温度下纯水中的c(H+)=c(OH-)= ![]() =1×10-6mol/L,故答案为:1×10-6mol/L;
=1×10-6mol/L,故答案为:1×10-6mol/L;
⑷①如果醋酸为强酸,全部电离,则1mol·L-1的CH3COOH溶液中c(H+)=1 mol·L-1,而1mol·L-1的CH3COOH溶液中c(H+)=10-2mol·L-1,说明是弱酸即弱电解质,故①符合题意;
②CH3COOH可以任意比与H2O互溶,强弱电解质与溶解性没有联系,故②不符合题意;
③在相同条件下,CH3COOH溶液的导电性比盐酸弱,说明醋酸溶液中的离子浓度小于盐酸中的离子浓度,则说明醋酸为弱电解质,故③符合题意;
④10mL1mol/L的CH3COOH恰好与10mL1mol/L的NaOH溶液完全反应,强酸与弱酸都是按照方程式比例消耗,因此不能说明是弱电解质,故④不符合题意;
⑤同浓度同体积的醋酸和盐酸与Fe反应时,醋酸溶液中放出H2的速度慢,说明同浓度醋酸中的氢离子浓度小于盐酸中氢离子浓度,说明电离程度小,因此为弱电解质,故⑤符合题意;
⑥醋酸溶液中CH3COOH、CH3COO-、H+同时存在,弱电解质存在弱电解质分子,故⑥符合题意;所以可以证明它是弱电解质的是①③⑤⑥,故答案为:①③⑤⑥。

 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
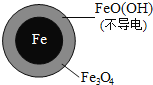
一课一练一本通系列答案【题目】用零价铁![]() 去除水体中的硝酸盐
去除水体中的硝酸盐![]() 已成为环境修复研究的热点之一.
已成为环境修复研究的热点之一.
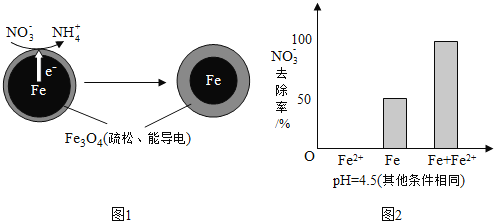
![]() 还原水体中
还原水体中![]() 的反应原理如图1所示.
的反应原理如图1所示.
①作负极的物质是______.
②正极的电极反应式是______.
![]() 将足量铁粉投入水体中,经24小时测定
将足量铁粉投入水体中,经24小时测定![]() 的去除率和pH,结果如下:
的去除率和pH,结果如下:
初始pH |
|
|
| 接近 |
|
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
![]() 时,
时,![]() 的去除率低.其原因是______.
的去除率低.其原因是______.
![]() 实验发现:在初始
实验发现:在初始![]() 的水体中投入足量铁粉的同时,补充一定量的
的水体中投入足量铁粉的同时,补充一定量的![]() 可以明显提高
可以明显提高![]() 的去除率.对
的去除率.对![]() 的作用提出两种假设:
的作用提出两种假设:
Ⅰ![]() 直接还原
直接还原![]() ;
;
Ⅱ![]() 破坏
破坏![]() 氧化层.
氧化层.
①做对比实验,结果如图2所示,可得到的结论是______.
②同位素示踪法证实![]() 能与
能与![]() 反应生成
反应生成![]() 结合该反应的离子方程式,解释加入
结合该反应的离子方程式,解释加入![]() 提高
提高![]() 去除率的原因:______.
去除率的原因:______.
![]() 其他条件与
其他条件与![]() 相同,经1小时测定
相同,经1小时测定![]() 的去除率和pH,结果如表:
的去除率和pH,结果如表:
初始pH |
|
|
| 约 | 约 |
1小时pH | 接近中性 | 接近中性 |
与![]() 中数据对比,解释
中数据对比,解释![]() 中初始pH不同时,
中初始pH不同时,![]() 去除率和铁的最终物质形态不同的原因:______.
去除率和铁的最终物质形态不同的原因:______.
【题目】甲烷催化裂解是工业上制备乙炔的方法之一。回答下列问题:
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-890 kJ·mol-1
C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l) ΔH2=-1 300 kJ·mol-1
O2(g)=2CO2(g)+H2O(l) ΔH2=-1 300 kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH3=-572 kJ·mol-1
则2CH4(g)![]() C2H2(g)+3H2(g) ΔH=________kJ·mol-1。
C2H2(g)+3H2(g) ΔH=________kJ·mol-1。
(2)某科研小组尝试利用固体表面催化工艺进行CH4的裂解。
①若用![]() 和
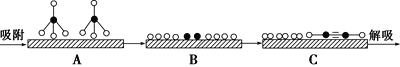
和![]() 分别表示CH4、C2H2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程如图所示。从吸附到解吸的过程中,能量状态最低的是________(填字母)。
分别表示CH4、C2H2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程如图所示。从吸附到解吸的过程中,能量状态最低的是________(填字母)。
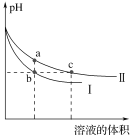
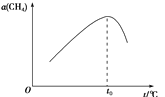
②在恒容密闭容器中充入a mol甲烷,测得单位时间内在固体催化剂表面CH4的转化率[α(CH4)]与温度(t)的关系如图所示,t0 ℃后CH4的转化率突减的原因可能是_______。
(3)甲烷分解体系中几种气体的平衡分压(p,单位为Pa)与温度(t,单位为℃)的关系如图所示:
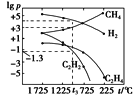
①t1 ℃时,向V L恒容密闭容器中充入0.12 mol CH4,只发生反应2CH4(g)![]() C2H4(g)+2H2(g),达到平衡时,测得p(C2H4)=p(CH4),CH4的平衡转化率为________。(保留3位有效数字)若改变温度至t2 ℃,CH4以0.01mol/(L· s)的平均速率增多,则t1________t2(填“>”“=”或“<”)。
C2H4(g)+2H2(g),达到平衡时,测得p(C2H4)=p(CH4),CH4的平衡转化率为________。(保留3位有效数字)若改变温度至t2 ℃,CH4以0.01mol/(L· s)的平均速率增多,则t1________t2(填“>”“=”或“<”)。
②在图中,t3 ℃时,化学反应2CH4(g)![]() C2H2(g)+3H2(g)的压强平衡常数Kp=____。
C2H2(g)+3H2(g)的压强平衡常数Kp=____。
(4)工业上,以石墨为电极,电解亚铁氰化钾K4[Fe(CN)6]溶液可以制备铁氰化钾{K3[Fe(CN)6],可用于检验Fe2+},阳极的电极反应式为____________。
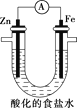
(5)设计如图实验探究牺牲阳极的阴极保护法原理:
操作 | 现象 |
(i)取铁极附近的溶液于试管中,滴加铁氰化钾溶液 | 无明显现象 |
(ii)在U形管铁极附近滴加铁氰化钾溶液 | 产生蓝色沉淀 |
得出结论:①锌______保护铁;(填“能”或“不能”)
②产生蓝色沉淀可以得出铁被铁氰化钾氧化生成______。