题目内容
下表为元素周期表的一部分,回答下列问题:
(1)写出元素符号:①
(2)若用M代表碱金属元素,则其最高价氧化物对应的水化物的化学式为
(3)在元素③与⑩中,化学性质较活泼的是
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | (11) | (12) |
N
N
,④Mg
Mg
,⑥Si
Si
,⑦S
S
.(2)若用M代表碱金属元素,则其最高价氧化物对应的水化物的化学式为
MOH
MOH
;若用X表示卤族元素,则其气态氢化物的分子式为HX
HX
;元素②、⑧、(12)的气态氢化物的稳定性由强到弱的顺序为HF>HCl>HBr
HF>HCl>HBr
(填化学式).(3)在元素③与⑩中,化学性质较活泼的是
K
K
(填元素符号),写出用化学实验证明它较活泼的方法:钾与水的反应比钠与水的反应更剧烈
钾与水的反应比钠与水的反应更剧烈
.分析:由元素在周期表中的位置可知,①为N,②为F,③为Na,④为Mg,⑤为Al,⑥为Si,⑦为S,⑧为Cl,⑨为Ar,⑩为K,(11)为Ca,(12)为Br.
(1)由推出的元素书写其元素符号;
(2)碱金属元素的最高化合价为+1价,卤族元素的最低化合价为-1价,元素②、⑧、(12)位于同一主族,随原子序数增大,非金属性减弱,则气态氢化物的稳定性减弱;
(3)③与⑩位于同一主族,随原子序数的增大,金属性增强.
(1)由推出的元素书写其元素符号;
(2)碱金属元素的最高化合价为+1价,卤族元素的最低化合价为-1价,元素②、⑧、(12)位于同一主族,随原子序数增大,非金属性减弱,则气态氢化物的稳定性减弱;
(3)③与⑩位于同一主族,随原子序数的增大,金属性增强.
解答:解:由元素在周期表中的位置可知,①为N,②为F,③为Na,④为Mg,⑤为Al,⑥为Si,⑦为S,⑧为Cl,⑨为Ar,⑩为K,(11)为Ca,(12)为Br.
(1)由上述分析可知,①为N,④为Mg,⑥为Si,⑦为S,故答案为:N;Mg;Si;S;
(2)碱金属元素的最高化合价为+1价,则最高价氧化物对应的水化物的化学式为MOH,卤族元素的最低化合价为-1价,则气态氢化物的分子式为HX,元素②、⑧、(12)位于同一主族,随原子序数增大,非金属性减弱,则气态氢化物的稳定性减弱,所以稳定性由强到弱的顺序为HF>HCl>HBr,
故答案为:MOH;HX;HF>HCl>HBr;
(3)③与⑩位于同一主族,随原子序数的增大,金属性增强,所以K的活泼性强,可利用钾与水的反应比钠与水的反应更剧烈来证明,
故答案为:K;钾与水的反应比钠与水的反应更剧烈.
(1)由上述分析可知,①为N,④为Mg,⑥为Si,⑦为S,故答案为:N;Mg;Si;S;
(2)碱金属元素的最高化合价为+1价,则最高价氧化物对应的水化物的化学式为MOH,卤族元素的最低化合价为-1价,则气态氢化物的分子式为HX,元素②、⑧、(12)位于同一主族,随原子序数增大,非金属性减弱,则气态氢化物的稳定性减弱,所以稳定性由强到弱的顺序为HF>HCl>HBr,
故答案为:MOH;HX;HF>HCl>HBr;
(3)③与⑩位于同一主族,随原子序数的增大,金属性增强,所以K的活泼性强,可利用钾与水的反应比钠与水的反应更剧烈来证明,
故答案为:K;钾与水的反应比钠与水的反应更剧烈.
点评:本题考查元素周期表和元素周期律,明确元素在周期表中的位置及同主族元素性质的变化规律即可解答,题目难度不大.

练习册系列答案
相关题目








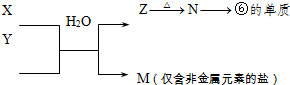
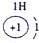
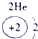
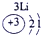
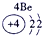
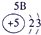
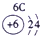
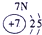
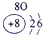
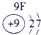
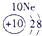
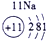





 表示的是
表示的是