题目内容
9.下列递变规律正确的是( )| A. | 原子半径:O<S<Na | |
| B. | 碱性强弱:LiOH>KOH>CsOH | |
| C. | 还原性:HCl>HBr>HI | |
| D. | 热稳定性:H2O<NH3<SiH4的依次增强 |
分析 A.原子电子层数越多,其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
B.元素的金属性越强,其最高价氧化物的水化物碱性越强;
C.元素的非金属性越强,其氢化物的还原性越弱;
D.元素的非金属性越强,其氢化物的稳定性越强.
解答 解:A.原子电子层数越多,其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,S、Na有3个电子层且S原子序数大于Na,O原子有2个电子层,所以原子半径Na>S>O,故A正确;
B.元素的金属性越强,其最高价氧化物的水化物碱性越强,金属性Cs>K>Li,所以碱性LiOH<KOH<CsOH,故B错误;
C.元素的非金属性越强,其氢化物的还原性越弱,非金属性Cl>Br>I,所以还原性:HCl<HBr<HI,故C错误;
D.元素的非金属性越强,其氢化物的稳定性越强,非金属性O>N>Si,所以氢化物的稳定性H2O>NH3>SiH4,故D错误;
故选A.
点评 本题考查元素周期律,侧重考查同一周期、同一主族元素原子结构与性质关系,明确元素周期律内涵是解本题关键,知道金属性、非金属性强弱判断方法,题目难度不大.

练习册系列答案
相关题目
20.原子序数为83的元素位于:①第5周期;②第6周期;③ⅣA族;④ⅤA族;⑤ⅡB族.其中正确的组合是( )
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ①⑤ |
17.某元素的原子核外有三个电子层,其中M电子数是L层电子数的一半,则此元素( )
| A. | C | B. | Si | C. | S | D. | C1 |
14.下列条件下的反应,放出H2最快的是( )
| 金属(粉末状)/mol | 酸的浓度和体积(mL) | 反应温度 | |||
| A | Mg | 0.1 | 3mol/L HCl | 10 | 20℃ |
| B | Al | 0.1 | 3mol/L HCl | 10 | 20℃ |
| C | Mg | 0.1 | 3mol/L CH3COOH | 10 | 20℃ |
| D | Mg | 0.1 | 3mol/L HNO3 | 10 | 30℃ |
| A. | A | B. | B | C. | C | D. | D |
18.以下反应属于吸热反应的是( )
| A. | 生石灰加水制熟石灰 | B. | 化石燃料的燃烧 | ||
| C. | 氢氧化钠溶液中滴加稀盐酸 | D. | 二氧化碳与高温的炭 |
19.已知五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族.A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子.下列说法正确的是( )
| A. | D元素最高价氧化物对应的水化物化学式H2YO4 | |
| B. | 原子半径由大到小的顺序为:B>D>E | |
| C. | B、C两种元素的气态氢化物中,C的气态氢化物较稳定 | |
| D. | A与B形成的两种化合物中,阴、阳离子物质的量之比均为1:2 |
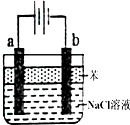 (1)用惰性电极电解饱和食盐水的反应方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.
(1)用惰性电极电解饱和食盐水的反应方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.