��Ŀ����
����Ŀ��ijС��ͬѧ������ͼװ�öԵ���Ȼ�ͭʵ��������о���
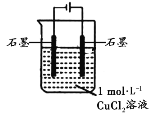
װ�� | ���� |
| ���һ��ʱ��ʱ������ʯī����������壬����ʯī�ϸ��ź�ɫ���ʣ��ձ��ڱ��ȣ���Һ����ɫ��Ϊ��ɫ |
��1������Ϊ������������������ ����Һ���̵�ԭ��д�����������ʵĵ缫��Ӧʽ�� ��
��2���Ҳ������ϣ�CuCl2��Һ�д���ƽ�⣺Cu2+ + 4Cl��![]() [CuCl4]2��(��ɫ) ��H��0���ݴ�����Ϊ:�������У�[CuCl4]2��(��ɫ)Ũ��������CuCl2��ɫ��Һ��ϳ���ɫ��������ƽ���ƶ�ԭ���Ʋ��ڵ�������[CuCl4]2��Ũ�������ԭ�� ��
[CuCl4]2��(��ɫ) ��H��0���ݴ�����Ϊ:�������У�[CuCl4]2��(��ɫ)Ũ��������CuCl2��ɫ��Һ��ϳ���ɫ��������ƽ���ƶ�ԭ���Ʋ��ڵ�������[CuCl4]2��Ũ�������ԭ�� ��
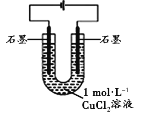
��3����������ͼװ�ã�����ͬ�����µ��CuCl2��Һ������Һ��ɫ�������̽����
װ�� | ���� |
| �����ͬʱ��ʱ������ʯī����������ݣ���Һ��Ϊ��ɫ������ʯī�ϸ��ź�ɫ���ʣ���Һ����ɫ��Ϊ��ɫ��U�ܱ��ȣ���ȴ������������Һ��Ϊ��ɫ |
��ͨ�����������֤ʵ�˼��ҵĹ۵��������Һ���̵���Ҫԭ���������� �����ҵ������� ��
��4���������������ϣ�
i. ���CuCl2��Һʱ���ܲ���[CuCl2]����[CuCl2]������Cu2+��ʻ�ɫ
ii. ϡ�ͺ�[CuCl2]������Һ����CuCl��ɫ�����ݴ˱���Ϊ���������У�����[CuCl2]������Cu2+��ʻ�ɫ����CuCl2��ɫ��Һ��ϳ���ɫ��
����������ʵ�飺
a��ȡ������ɫ��Һ2 mL����20 mLˮϡ�ͣ�����5���Ӻ���Һ�в�����ɫ������
b. ��ȡ�����Ȼ�ͭ�����ͭ�ۣ������м�2 mLŨ���ᣬ���Ȼ�ú�[CuCl2]���Ļ�ɫ��Һ��
c. ��ȴ����������Һ����
d. ȡc��2 mL��Һ����20 mLˮϡ�ͣ�����5���Ӻ���Һ�в�����ɫ������
�� a��Ŀ���� ��
�� д��b������[CuCl2]�������ӷ���ʽ�� ��
�� ����c�б�Ҫ�IJ��������� ��
���ݴ˵ó����ۣ����ʱ������������[CuCl2]���ǵ�����Һ���̵�ԭ��
���𰸡�
��1��Cl2��2Cl��-2e��= Cl2��
��2�������̷��ȵ����¶����ߣ�Cu2+ + 4Cl��![]() [CuCl4]2�������ƶ���
[CuCl4]2�������ƶ���
��3������������Һ��Ϊ��ɫ��U����ȴ������������Һ��Ϊ��ɫ��
��4����֤��������ʵ�������£��������ɫ��Һ�д���[CuCl2]����
��Cu2+ + 4Cl��+ Cu = 2[CuCl2]����
�ۼ���CuCl2��ɫ��Һ��ֱ����Һ��ɫ�������ɫ��Һ������ͬ��
��������
�����������1������������������������Ӧ����Һ�е������ӷŵ�������������������ˮ����Һ���ܳ�����ɫ���ʴ�Ϊ��Cl2��2Cl��-2e��= Cl2����
��2�������̷��ȵ����¶����ߣ�Cu2+ + 4Cl��![]() [CuCl4]2�������ƶ���[CuCl4]2��Ũ�����ʴ�Ϊ�������̷��ȵ����¶����ߣ�Cu2+ + 4Cl��
[CuCl4]2�������ƶ���[CuCl4]2��Ũ�����ʴ�Ϊ�������̷��ȵ����¶����ߣ�Cu2+ + 4Cl��![]() [CuCl4]2�������ƶ���
[CuCl4]2�������ƶ���
��3������������������������������Һ��Ϊ��ɫ��˵����������������Ե����Cu2+ + 4Cl��![]() [CuCl4]2��(��ɫ) ��H��0���¶Ƚ��ͣ�ƽ�������ƶ�����ҺӦ�ó��ֻ�ɫ����U����ȴ������������Һ��Ϊ��ɫ������ҵ��ƶ�Ҳ����ȷ���ʴ�Ϊ������������Һ��Ϊ��ɫ��U����ȴ������������Һ��Ϊ��ɫ��
[CuCl4]2��(��ɫ) ��H��0���¶Ƚ��ͣ�ƽ�������ƶ�����ҺӦ�ó��ֻ�ɫ����U����ȴ������������Һ��Ϊ��ɫ������ҵ��ƶ�Ҳ����ȷ���ʴ�Ϊ������������Һ��Ϊ��ɫ��U����ȴ������������Һ��Ϊ��ɫ��
��4����������Ϣ��ȡ������ɫ��Һ2 mL����20 mLˮϡ�ͣ�����5���Ӻ���Һ�в�����ɫ������˵���������ɫ��Һ�д���[CuCl2]�����ʴ�Ϊ��֤��������ʵ�������£��������ɫ��Һ�д���[CuCl2]����
���Ȼ�ͭ�����ͭ�ۼ���2 mLŨ�����У����Ȼ�ú�[CuCl2]���Ļ�ɫ��Һ����Ӧ�����ӷ���ʽΪCu2+ + 4Cl��+ Cu = 2[CuCl2]�����ʴ�Ϊ��Cu2+ + 4Cl��+ Cu = 2[CuCl2]����
��c�IJ������֤�����ʱ������������[CuCl2]���ǵ�����Һ���̵�ԭ�����������������Ϊ����CuCl2��ɫ��Һ��ֱ����Һ��ɫ�������ɫ��Һ������ͬ���ʴ�Ϊ������CuCl2��ɫ��Һ��ֱ����Һ��ɫ�������ɫ��Һ������ͬ��

����Ŀ�������£���100 mL 0.1 mol/L NH4Cl��Һ�м����������ʡ��йؽ�����ȷ����
��������� | ���� | |
A�� | 100 mL 0.1 mol/L���� | ��Һ��2c(NH4+)=" " c(Cl��) |
B�� | 0.01 mol Na2O2���� | ��Ӧ��ȫ����ҺpH����c(Na��) = 2c(Cl��) |
C�� | 100 mL H2O | ��ˮ�������c(H��)c(OH��)���� |
D�� | 100 mL 0.1 mol/L NH3H2O | ��Һ�� |
A. A B. B C. C D. D