题目内容
【题目】实验室用下面装置测定FeO和Fe2O3固体混合物中Fe2O3的质量,D装置的硬质双通玻璃管中的固体物质是FeO和Fe2O3的混合物。
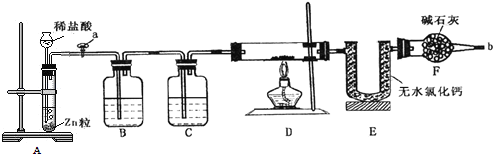
(1)实验前如何检验装置A的气密性________________________________________;
(2)为了实验安全,在点燃酒精灯前,在F装置出口b处必须_____________________;
(3)装置C中盛装的液体是浓硫酸,则装置B的作用是_________________________;
(4)U形管E右边又连接干燥管F的目的是___________。
(5)若FeO和Fe2O3固体混合物的质量为23.2 g,反应完全后U形管的质量增加7.2 g,则混合物中Fe2O3的质量为________g。
【答案】先开启旋塞a,向长颈漏斗中加水,当水面超过长颈漏斗下口时,关闭旋塞a,继续加水,使水上升到长颈漏斗中,静置片刻,若水面不下降,则说明装置气密性良好 验纯 除去H2中的HCl 防止空气中的水蒸气被U型管内的无水氯化钙吸收,引起实验误差 16.0
【解析】
(1)检验装置A的气密性时,应创设一个密闭环境,通过往长颈漏斗内加水,看水面是否下降,判断气密性是否良好;
(2)为了防止氢气不纯,点燃时发生爆炸,在点燃酒精灯前,在F装置出口b处必须验验H2的纯度;
(3)装置C中盛装的液体是浓硫酸,则装置B的作用是把H2中混有的HCl除掉;
(4)U形管E右边又连接干燥管F的目的是防止燃烧生成的水进行U型管内;
(5)先求出生成水的物质的量,从而求出混合物中氧原子的物质的量,然后假设未知数,利用质量和为23.2g,建立等量关系式,从而求出Fe2O3的质量。
(1)检验装置A的气密性时,应先开启旋塞a,向长颈漏斗中加水,当水面超过长颈漏斗下口时,关闭旋塞a,继续加水,使水上升到长颈漏斗中,静置片刻,若水面不下降,则说明装置气密性良好;
(2)为了实验安全,在点燃酒精灯前,在F装置出口b处必须验验H2的纯度,以防爆炸事故的发生;
(3)装置C中盛装的液体是浓硫酸,则装置B的作用是除去H2中的HCl。答案为:除去H2中的HCl;
(4)U形管E右边又连接干燥管F的目的是防止燃烧生成的水被U型管内的无水氯化钙吸收,引起实验误差。答案为:防止燃烧生成的水被U型管内的无水氯化钙吸收,引起实验误差;
(5)n(H2O)=![]() =0.4mol,则混合物中的n(O)=0.4mol,
=0.4mol,则混合物中的n(O)=0.4mol,
设Fe2O3的物质的量为x mol,则FeO的物质的量为(0.4-3x)mol,
72(0.4-3x)+160x=23.2
x=0.1mol,m(Fe2O3)=0.1mol×160g/mol=16.0g。

 中考解读考点精练系列答案
中考解读考点精练系列答案【题目】下图是元素周期表的一部分:
① | |||||||||||||||||
④ | ⑤ | ⑥ | |||||||||||||||
② | ③ | ⑦ | ⑧ | ||||||||||||||
Fe | |||||||||||||||||
Ⅰ.用化学用语回答下列问题:
(1)①、②、⑥形成的化合物中存在的化学键类型有________。
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_______。
(3)写出②的离子结构示意图为__________。
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。Y的水溶液与洁厕灵混合使用会产生一种有毒气体,该反应的离子方程式为_______。
Ⅱ.A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
![]()
(1)若A是一种金属单质,C是淡黄色固体,写出C的一种用途_____;
(2)若A、B、C均为化合物且含有同一种金属元素,D是会造成温室效应的一种气体,请写出D的电子式_____,A和C反应的离子方程式 ___。
(3)若D是一种常见的过渡金属单质,原子核内有26个质子,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的方法是________;又知在酸性溶液中该金属离子能被双氧水氧化,写出该反应的离子方程式_________。