题目内容
【题目】某化学兴趣小组试利用镁铝合金废料(不含其它杂质)制备硫酸铝晶体,其实验流程如图:
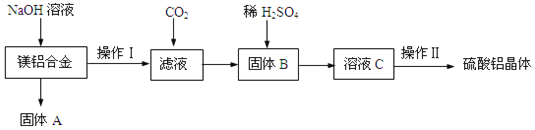
(1)在镁铝合金中加入NaOH溶液,发生反应的离子反应方程式为_____,固体B的化学式_____。
(2)操作Ⅱ包含的实验步骤有:_____、冷却结晶、过滤、洗涤、干燥。
(3)若初始时称取的镁铝合金废料的质量为7.65 g,得到固体A的质量为3.6 g,硫酸铝晶体的质量为49.95 g(假设每一步的转化率均为100%)。计算所得硫酸铝晶体的化学式为_____。( 在答题卷上写出计算过程)
(4)另取7.65 g该镁铝合金废料溶于400mL 3mol/L盐酸后,滴入3mol/LNaOH溶液,使所得沉淀中的Al(OH)3完全溶解,则滴入NaOH溶液的体积最少为_____mL(在答题卷上写出计算过程)。
【答案】2Al+2NaOH+2H2O=2NaAlO2+3H2↑ Al(OH)3 蒸发浓缩 Al2(SO4)318H2O 450
【解析】
向镁铝合金中加入足量氢氧化钠溶液,发生反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,镁不反应,固体A为Mg,采用过滤的方法进行分离,向滤液中通入二氧化碳,使偏铝酸钠转化为氢氧化铝沉淀,再通过过滤进行分离,固体B为氢氧化铝,氢氧化铝与硫酸反应得到硫酸铝溶液,再经过蒸发浓缩、冷却结晶、洗涤、干燥得到硫酸铝晶体;据此分析。
(1)Al和氢氧化钠溶液生成可溶性的偏铝酸钠与氢气,镁不反应,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,由上述分析可知,固体B为Al(OH)3,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;Al(OH)3;
(2)从溶液中获得晶体,需要经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作,故答案为:蒸发浓缩;
(3)Al的质量为7.65g-3.6g=4.05g,其物质的量为![]() =0.15mol,设硫酸铝晶体化学式为:Al2(SO4)3nH2O,根据Al元素守恒,硫酸铝晶体的物质的量为
=0.15mol,设硫酸铝晶体化学式为:Al2(SO4)3nH2O,根据Al元素守恒,硫酸铝晶体的物质的量为![]() =0.075mol,故硫酸铝晶体的相对分子质量为
=0.075mol,故硫酸铝晶体的相对分子质量为![]() =666,则54+96×3+18n=666,解得n=18,故该硫酸铝晶体的化学式为:Al2(SO4)318H2O,故答案为:Al2(SO4)318H2O;
=666,则54+96×3+18n=666,解得n=18,故该硫酸铝晶体的化学式为:Al2(SO4)318H2O,故答案为:Al2(SO4)318H2O;
(4)Mg的质量为3.6g,其物质的量为0.15mol,Al的质量为4.05g,其物质的量为0.15mol,若该Mg、Al混合物溶于400mL 3mol/L盐酸后,n(HCl)=0.4L×3mol/L=1.2mol,消耗n(HCl)=2n(Mg)+3n(Al)=2×0.15mol+3×0.15mol=0.75mol,剩余HCl为1.2mol-0.75mol=0.45mol,滴入NaOH溶液,使所得沉淀中无Al(OH)3,则发生H++OH﹣=H2O,Mg2++2OH﹣=Mg(OH)2↓、Al3++4OH﹣=AlO2﹣+2H2O,则需要n(NaOH)=n(HCl)+2n(Mg)+4n(Al)=0.45mol+2×0.15mol+4×0.15mol=1.35mol,V(NaOH)=![]() =0.45L=450mL,故答案为:450。
=0.45L=450mL,故答案为:450。

【题目】工业上用闪锌矿(主要成分为ZnS,还含有CdS、Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:(已知Cd的金属活动性介于Zn和Fe之间)
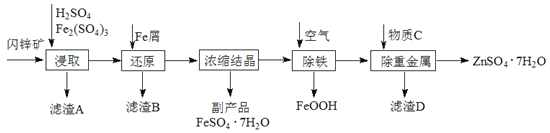
(1)从滤渣A中可获得一种淡黄色非金属单质的副产品,其化学式为________。
(2)浸取过程中Fe2(SO4)3的作用是_______________,浸取时Fe2(SO4)3与ZnS发生反应的化学方程式为____________________________________________。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为_______________________。该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是____________________________________。
(4)置换法除重金属离子是Cd2+,所用物质C为_________。
(5)硫酸锌的溶解度与温度之间的关系如下表:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
从除重金属后的硫酸锌溶液中获得硫酸锌晶体的实验操作为__________、__________、过滤、干燥。
【题目】下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是
| 甲 | 乙 | 丙 |
A | Al | HCl | NaOH |
B | NH3 | O2 | HNO3 |
C | SiO2 | NaOH | HF |
D | SO2 | Ca(OH)2 | NaHCO3 |
A.AB.BC.CD.D