题目内容
【题目】如图为相互串联的甲乙两个电解池,请回答:
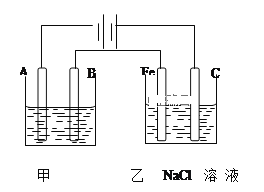
(1)甲池若为用电解原理精炼铜的装置,A极是__极,材料是___,B极电极反应方程式为___。
(2)乙池中若滴入少量酚酞试液,开始一段时间后,___极(填“Fe”或“C”)附近变红色。
(3)若乙槽阳极放出气体在标准状况下的体积为2.24L,
①甲槽阴极增重___g。
②若乙槽电解后得到碱液的物质的量浓度为2moL/L,则乙槽剩余液体体积为__mL。
【答案】阴 精铜或纯铜 Cu-2e-=Cu2+ Fe 6.4 100
【解析】
(1)甲池若为用电解原理精炼铜的装置,A极与电源负极相连,应为阴极。答案为:阴;
因为此电池是精炼铜的装置,所以阴极材料为精铜。答案为:精铜或纯铜;
B极为阳极,电极反应方程式为Cu-2e-=Cu2+。答案为:Cu-2e-=Cu2+
(2)乙池中,阴极的电极反应式为:2H2O+2e-=2OH-+H2↑;
若滴入少量酚酞试液,开始一段时间后,阴极即Fe电极附近变红色。
答案为:Fe;
(3)乙槽中阳极发生的反应为:2Cl--2e- =Cl2↑,若放出气体在标准状况下的体积为2.24L,
则失去的电子为0.2mol。
①甲槽阴极反应为Cu2++2e-=Cu,依据电子守恒,生成Cu 0.1mol,质量为6.4g。
答案6.4;
②在乙槽中,得到的碱液为NaOH,其物质的量为:
![]() ,
,
![]()
答案为:100。

练习册系列答案
相关题目