题目内容
【题目】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知A、I为常见金属单质,B、H为固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。
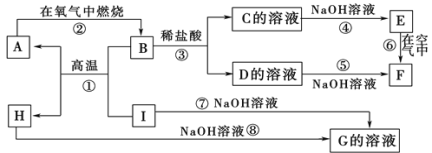
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是______,H的化学式为_______。
(2)反应③的离子方程式为 ____________,向G中通少量CO2的离子方程式为__________。
(3)反应⑥化学方程式___________。
(4)C中阳离子检验方法:______。
(5)1mol I发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准况下占______L。
【答案】铁元素 Al2O3 Fe3O4+8H+=2Fe3++Fe2+ +4H2O 2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32— 4Fe(OH)2 + O2 + 2H2O=4Fe(OH)3 取C中溶液少许于试管中,先滴加少量KSCN溶液无现象,在通入氯气(或滴加氯水,或滴加双氧水),溶液变血红色,则说明含有二价铁离子。(或用铁氰化钾溶液检验生成特征蓝色沉淀) 33.6
【解析】
由F是红褐色难溶于水的沉淀可知,F为Fe(OH)3,由A、B、C、D、E、F六种物质中均含同一种元素和题给转化关系可知A为铁、B为四氧化三铁、C为氯化亚铁、D为氯化铁;由四氧化三铁和I反应生成铁和H及I、H均能与氢氧化钠溶液反应可知,I为Al、H为氧化铝、G为偏铝酸钠。
(1)由分析可知,A、B、C、D、E、F六种物质中均含铁元素,H为氧化铝,故答案为:铁元素;Al2O3;
(2)反应③为四氧化三铁和盐酸反应生成氯化铁、氯化亚铁和水,反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2+ +4H2O;偏铝酸钠溶液与少量二氧化碳反应生成氢氧化铝沉淀和碳酸钠,反应的离子方程式为2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32—,故答案为:Fe3O4+8H+=2Fe3++Fe2+ +4H2O;2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32—;
(3)反应⑥为氢氧化亚铁与空气中的氧气反应生成氢氧化铁,反应的化学方程式为4Fe(OH)2 + O2 + 2H2O=4Fe(OH)3,故答案为:4Fe(OH)2 + O2 + 2H2O=4Fe(OH)3;
(4)C溶液为氯化亚铁溶液,检验亚铁离子的方法是取氯化亚铁中溶液少许于试管中,先滴加少量KSCN溶液无现象,在通入氯气(或滴加氯水,或滴加双氧水),溶液变血红色,则说明含有二价铁离子(或用铁氰化钾溶液检验生成特征蓝色沉淀),故答案为:取C中溶液少许于试管中,先滴加少量KSCN溶液无现象,在通入氯气(或滴加氯水,或滴加双氧水),溶液变血红色,则说明含有二价铁离子。(或用铁氰化钾溶液检验生成特征蓝色沉淀);
(5)铝高温条件下与四氧化三铁反应生成铁和氧化铝,反应生成的铁与水蒸气反应生成四氧化三铁和氢气,由方程式可得Al—![]() Fe—
Fe—![]() H2,则1mol I发生反应后生成的A高温下与足量的水蒸气反应生成标准况下氢气的体积为
H2,则1mol I发生反应后生成的A高温下与足量的水蒸气反应生成标准况下氢气的体积为![]() mol×22.4L/mol=33.6L,故答案为:33.6。
mol×22.4L/mol=33.6L,故答案为:33.6。